
| 气体 | 反应前的药品状态 | 反应条件 | 气体性质 |
| 甲 | 固体+液体 | 常温 | 不与水反应,不易溶于水,密度比空气大 |
| 乙 | 固体+固体 | 加热 | 能与水发生反应,极易溶于水,密度比空气小 |
| 丙 | 固体+液体 | 加热 | 能与水发生反应,能溶于水,密度比空气大 |
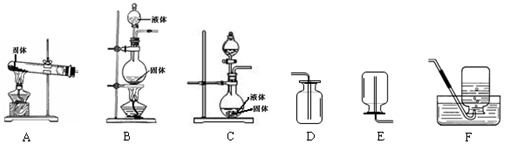
分析 (1)根据表中的信息及气体发生和收集装置的选择依据回答.
(2)根据实验室要制取和收集甲气体的性质并结合实验室制取氧气、氢气、二氧化碳的反应原理回答.
(3)根据氨气的实验室制法以及发生装置和收集装置的选择条件即可.
解答 解:(1)A装置属于固体加热型,反应物均为固体,反应条件是加热,故能用发生装置A 制取的气体是乙.故填:乙;
(2)甲气体不易溶于水,密度大于空气,氧气具有此性质,制取方法是利用固体和液体在常温下反应,说明是实验室用过氧化氢制氧气,方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)由资料知:加热氯化铵和氢氧化钙固体混合物可制取氨气,所以选择装置A来制取,因为氨水极易溶于水,不可采用排水法收集,而其密度比空气小,可用向下排空气法,故答案为:A;E.
点评 本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取气体的反应原理、发生装置和收集装置的选择依据等是正确解答本题的关键.


科目:初中化学 来源: 题型:选择题
| A. | 回收废旧塑料减少白色污染 | |
| B. | 提倡使用私家车出行 | |
| C. | 大量使用化肥农药提高农作物的产量 | |
| D. | 将工厂排放废弃的烟囱加高 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
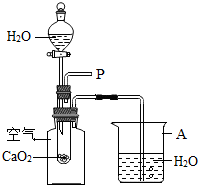 小明在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小明共同探究.
小明在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小明共同探究.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧气可用于生物呼吸 | B. | 活性炭可用于除去冰箱中的异味 | ||
| C. | 铜丝可用作导线 | D. | 干冰可用于人工降雨 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
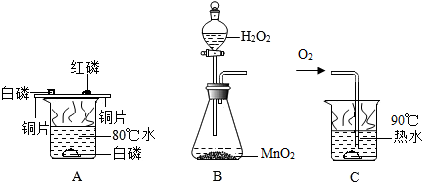
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 氧化铁 | 氧化铝 | 氧化铜 | 氧化镁 | |
| 开始反应 | 420 | 515 | 305 | 490 |
| 剧烈反应 | 490 | 540 | 350 | 545 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 药品柜编号 | ① | ② | ③ | ④ | ⑤ |
| 药品 | 氢氧化钠 氢氧化钙 | 盐酸 硫酸 | 二氧化锰 氧化铜 | 氯化钠 硫酸铜 | 锌粒 铜片 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验操作 |  |  |  |
| 实验现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变为蓝色 | 无明显现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com