
| 加入的稀盐酸(g) | 20 | 40 | 60 |
| 生成气体的质量(g) | 2.2 | 4.4 | 4.4 |
分析 加入盐酸到40g时生成的二氧化碳是4.4g,加入60g稀盐酸时二氧化碳还是4.4g,说明只生成二氧化碳4.4g,所以根据二氧化碳的质量和对应的化学方程式求算碳酸钠的质量,进而求算其质量分数.
解答 解:由于加入40g和60g稀盐酸得到的二氧化碳都是4.4g,所以只生成4.4g二氧化碳.
设参加反应的碳酸钠的质量为x,
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
x 4.4g
$\frac{106}{44}$=$\frac{x}{4.4g}$
x=10.6g
该混合液中碳酸钠的质量分数为$\frac{10.6g}{50g}$×100%=21.2%
答:(1)当混合液中的碳酸钠完全反应时,生成气体的质量为4.4g.
(2)该混合液中碳酸钠的质量分数为21.2%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


科目:初中化学 来源: 题型:选择题
| A. |  水的电解 | |
| B. | 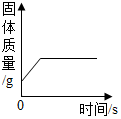 将一定质量硫酸铜溶液倒入盛有铁钉的烧杯 | |
| C. |  加热一定量KMnO4固体 | |
| D. | 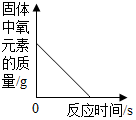 向少量的H2O2溶液中加入MnO2固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 向一定量的NaOH溶液中通入CO2后再滴加稀盐酸,有气体生成 | |
| B. | 向装有一定量NaOH溶液的烧杯中滴几滴酚酞溶液,再逐滴加入稀盐酸 | |
| C. | 先测定NaOH溶液的pH,再逐滴加入稀盐酸,溶液的pH数值逐渐降低 | |
| D. | 向装有少量稀盐酸的试管中滴加足量NaOH溶液,再向其中滴加Na2CO3溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
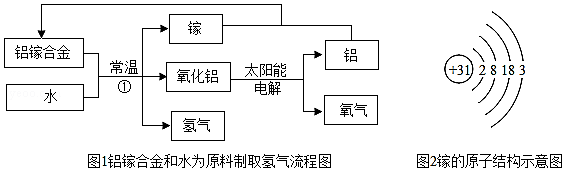
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
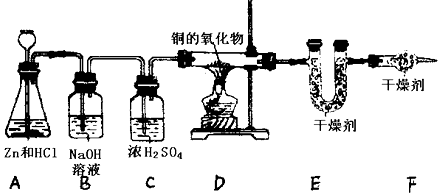
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
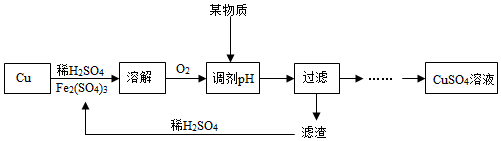
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com