
ЃЈ4ЗжЃЉЪЏгЂЕФжївЊГЩЗжЮЊЖўбѕЛЏЙшЃЌЦфЛЏбЇЪНЮЊSiO2ЁЃЫќЪЧВЃСЇЙЄвЕКЭЬеДЩЙЄвЕЕФдСЯЃЌвБН№ЙЄвЕЕФжњШлМСЁЃ
ЃЈ1ЃЉЖўбѕЛЏЙшЪєгк ЃЈЬюЁАЫсЁБЁЂЁАМюЁБЁЂЁАбЮЁБЁЂЁАбѕЛЏЮяЁБЛђЁАгаЛњЮяЁБжавЛжжЃЉЁЃ
ЃЈ2ЃЉзАгаЧтбѕЛЏФЦШмвКЕФЪдМСЦПВЛФмгУВЃСЇШћЃЌдвђЪЧдкГЃЮТЯТЃЌNaOHгыВЃСЇШћжаЕФSiO2ЛКТ§ЕиЗЂЩњЗДгІЩњГЩNa2SiO3КЭH2OЃЌNa2SiO3ЪЙЦППкгыЦПШћеГКЯдквЛЦ№ЃЌИУЗДгІЕФЛЏбЇЗНГЬЪНЮЊ ЁЃ
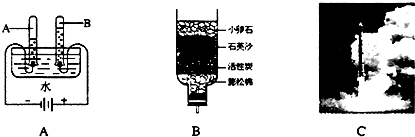
ЃЈ3ЃЉЙшЪЧЬЋбєФмЕчГиКЭЕчФдаОЦЌВЛПЩШБЩйЕФВФСЯЁЃЩњВњИпДПЙшЕФСїГЬЪОвтЭМШчЯТЃК
ЂйжЦБИДжЙшЕФЗДгІЮЊЃКSiO2+2CИпЮТ Si +2COЁќЃЌЗДгІЕФЛљБОРраЭЪЧ ЗДгІЃЈЬюЁАЗжНтЁБЁАЛЏКЯЁБЁАжУЛЛЁБЁАИДЗжНтЁБжЎвЛЃЉЁЃ
ЂкећИіжЦБИЙ§ГЬБиаыДяЕНЮоЫЎЮобѕЃЌШєдкH2ЛЙдSiHCl3Й§ГЬжаЛьШыO2ЃЌПЩФмв§Ц№ЕФКѓЙћЪЧ ЁЃ
ЃЈЙВ4ЗжЃЌУППе1ЗжЃЉЃЈ1ЃЉбѕЛЏЮяЃЈ2ЃЉ2NaOH + SiO2 = Na2SiO3+ H2OЃЈ3ЃЉЂйжУЛЛЂкЙшБЛбѕЛЏЕУВЛЕНИпДПЙшЃЌЧвЗЂЩњБЌеЈЃЈЦфжавЛЬѕМДПЩЃЉ
НтЮі:гЩСНжждЊЫизщГЩЕФЛЏКЯЮяЃЌШчЙћЦфжавЛжжЪЧбѕдЊЫиЃЌдђЫћЪЧбѕЛЏЮяЙЪЃЈ1ЃЉЬюбѕЛЏЮя
NaOHгыВЃСЇШћжаЕФSiO2ЛКТ§ЕиЗЂЩњЗДгІЩњГЩNa2SiO3КЭH2OЃЌЗДгІЮяКЭЩњГЩЮявбОИјГіЃЌдђАДееЪщаДЛЏбЇЗНГЬЪНЕФЙцдђМДПЩаДГі2NaOH + SiO2 = Na2SiO3+ H2O
гЩвЛжжЕЅжЪКЭвЛжжЛЏКЯЮяЗДгІЩњГЩСэвЛжжЕЅжЪКЭСэвЛжжЛЏКЯЮяЕФЗДгІЮЊжУЛЛЗДгІЃЌЙЪЃЈ3ЃЉЂйЬюжУЛЛ
ЧтЦјПЩвдШМЩеЃЌДяЕНЫќЕФБЌеЈМЋЯоМДПЩЗЂЩњБЌеЈЃЌЙшдкИпЮТЪБгабѕЦјЛсБЛбѕЛЏЃЌЙЪЃЈ3ЃЉЂкЬюЙшБЛбѕЛЏЕУВЛЕНИпДПЙшЃЌЧвЗЂЩњБЌеЈЃЈЦфжавЛЬѕМДПЩЃЉ


 ЭЌВНбЇЕфвЛПЮЖрСЗЯЕСаД№АИ
ЭЌВНбЇЕфвЛПЮЖрСЗЯЕСаД№АИ ОЕфУмОэЯЕСаД№АИ
ОЕфУмОэЯЕСаД№АИ Н№ХЦПЮЬУСЗЯЕСаД№АИ
Н№ХЦПЮЬУСЗЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃК
| ||
| ||
| ||
| ||
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com