
 一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )
一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )| A. | 丁是该反应的催化剂 | B. | 丙可能是单质 | ||
| C. | 该反应中甲、丙的质量比为7:10 | D. | 若消耗3g的乙,则生成17g的丙 |
分析 本题可分析甲~丁四种物质反应前后各物质的质量分数,确定是反应物还是生成物,据此结合题意进行分析判断即可.
解答 解:由四种物质反应前后各物质的质量分数可知,反应前后甲的质量分数减少了70%-42%=28%,故甲是反应物;同理可以确定乙的质量分数减少了14%-(1-42%-40%-10%)=6%,故乙是反应物;丙的质量分数增加了40%-(1-70%-14%-10%)=34%,丙是生成物;丁的质量分数不变,可能作该反应的催化剂,也可能没有参加反应.
A.丁的质量分数不变,可能没有参加反应,也可能作该反应的催化剂,故选项说法错误.
B.该反应的反应物为甲和乙,生成物是丙,属于化合反应,丙不可能是单质,故选项说法错误.
C.该反应中甲、丙的质量比为:28%:34%=14:17,故选项说法错误.
D.已知参加反应的乙与生成的丙的质量比为:6%:34%=3:17,所以若消耗3g的乙,则生成17g的丙,故正确.
故选D.
点评 本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析图中数据,灵活运用质量守恒定律.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:初中化学 来源: 题型:解答题
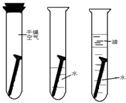 为探究铁锈蚀的影响因素,某兴趣小组做了如下实验.
为探究铁锈蚀的影响因素,某兴趣小组做了如下实验.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | HCl、NaOH、NaCl | B. | KNO3、NaCl、FeCl3 | ||
| C. | K2SO4、H2SO4、Na2CO3 | D. | NaOH、Na2CO3、NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②⑤⑥ | C. | ②③⑤ | D. | ②④⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
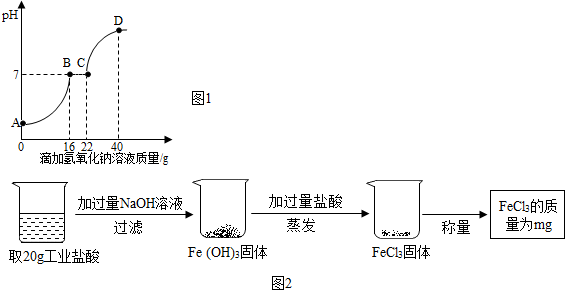
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
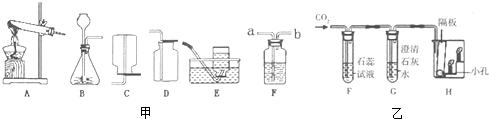
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 废液中有硫酸铜 | B. | 废液中至少有三种溶质 | ||
| C. | 废液中可能有硝酸银 | D. | 废液中可能有氯化钡 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com