
 �������Ƽ���ƵõĴ�����ͨ�������������Ȼ��ƣ�ijͬѧ��ⶨ���������Ȼ������ʵĴ�����Ʒ��̼���ƣ�Na2CO3����������������ͬѧ�������£��ֳ�ȡ6g���������ձ��в�����ϡ���ᣬ��ϡ����μ���36.5gʱ���ձ�����Һ��������Ϊ40.3g������������ȫ���ݳ�����������������������ϡ�����������ϵ��ͼ��ʾ�����ʴ����⣺
�������Ƽ���ƵõĴ�����ͨ�������������Ȼ��ƣ�ijͬѧ��ⶨ���������Ȼ������ʵĴ�����Ʒ��̼���ƣ�Na2CO3����������������ͬѧ�������£��ֳ�ȡ6g���������ձ��в�����ϡ���ᣬ��ϡ����μ���36.5gʱ���ձ�����Һ��������Ϊ40.3g������������ȫ���ݳ�����������������������ϡ�����������ϵ��ͼ��ʾ�����ʴ����⣺| 106 |
| x |
| 44 |
| 2.2g |
| 5.3g |
| 6g |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����
���� ���ֱ��ʾ��ͬ�����ԭ�ӣ�������ʾ��ͼ�п��Ա�ʾ��������ǣ�������
���ֱ��ʾ��ͬ�����ԭ�ӣ�������ʾ��ͼ�п��Ա�ʾ��������ǣ�������A�� |
B�� |
C��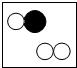 |
D�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
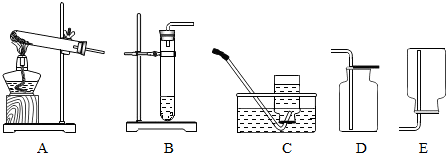
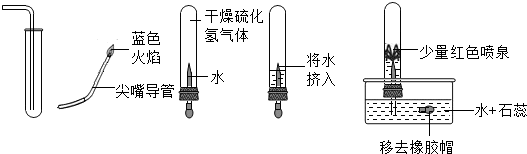
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��ѧ���� | 4S | Al3+ | ||
| ���ŵ����� | 2������������� | ����������Ԫ�صĻ��ϼ�Ϊ+3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com