
 “空气中氧气含量的测定”有多种方法.甲生设计了如图所示的实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.回答下列问题:
“空气中氧气含量的测定”有多种方法.甲生设计了如图所示的实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.回答下列问题:分析 空气成分测定实验的原理是:利用红磷燃烧消耗密闭容器内空气中的氧气,生成了能与水反应,体积可以忽略的白色固体,导致密闭容器中压强减小,通过观测进入容器中水的体积来确定空气中氧气的体积分数.已知氧气约占空气总体积的1/5,造成测量结果偏低的原因有:装置气密性不好,装置未冷却到室温就打开弹簧夹;若实验结果比实际偏高,可能是集气瓶内的部分空气散失造成的,主要原因有:点燃红磷后向集气瓶塞塞子时动作过缓,弹簧夹没有夹紧等.
解答 解:
(1)红磷燃烧消耗密闭容器内空气中的氧气,导致密闭容器中压强减小,从而使水进入集气瓶.故答案应为:瓶内氧气消耗导致瓶内压强变小;
(2)若实验过程中红磷用量不足,装置漏气,则会导致密闭容器内的氧气不能够被完全消耗,则会使进入容器内水的体积小于其容积的1/5,使测量结果比实际偏低.
若弹簧夹没有夹紧,会造成集气瓶内的部分空气散失,使进入集气瓶中水的量偏多.答案为:弹簧夹未夹紧;
答案为:
(1)瓶内氧气消耗导致瓶内压强变小;
(2)红磷不足;装置漏气;弹簧夹未夹紧.
点评 本题综合考查了空气成分的测定实验及本实验的误差分析,又综合考查了碱的化学性质.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
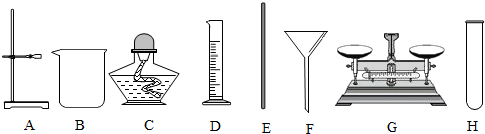
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
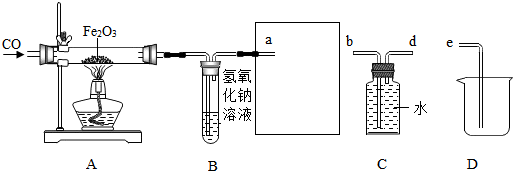
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
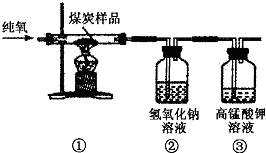 在我国的能源结构中,燃烧约占70%,它是由多种有机物和无机物组成的混合物,主要成分是碳.
在我国的能源结构中,燃烧约占70%,它是由多种有机物和无机物组成的混合物,主要成分是碳. ,该化学方程式中最后一个化学式因资料污损而模糊不全,请推测其化学式为H2SO4;反应中硫元素被氧化,化合价从反应前的+4价变为反应后的+6价.
,该化学方程式中最后一个化学式因资料污损而模糊不全,请推测其化学式为H2SO4;反应中硫元素被氧化,化合价从反应前的+4价变为反应后的+6价.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
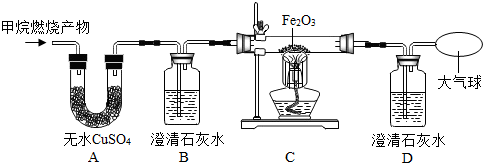
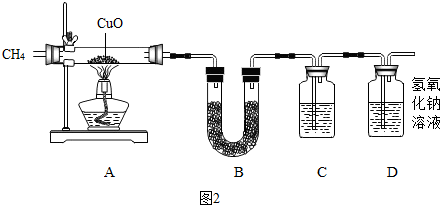
| A中玻璃管(含药品)质量 | 装置B的质量 | 装置C的质量 | |
| 反应前 | 150g | 156.6g | 256.8g |
| 反应后 | 147.2g | 158.4g | 257.9g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com