
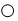 ”中填写的离子符号为H+;
”中填写的离子符号为H+;分析 氢氧化钠溶液显碱性,能使酚酞试液变红色,能和稀盐酸反应生成氯化钠和水;
稀盐酸能和锌反应生成氯化锌和氢气;
根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断.
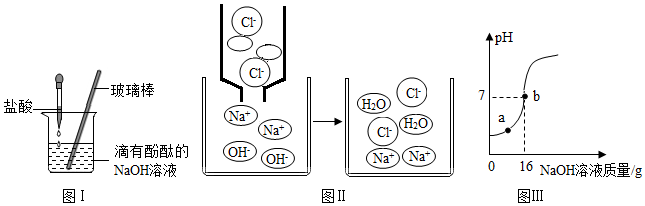
解答 解:(1)氢氧化钠和稀盐酸反应生成氯化钠和水,反应的化学方程式为:NaOH+HCl═NaCl+H2O.
故填:NaOH+HCl═NaCl+H2O.
(2)向烧杯中逐滴滴入盐酸至过量,在这个过程中,能够说明盐酸与氢氧化钠发生了化学反应的实验现象是溶液由红色变成无色.
故填:溶液由红色变成无色.
(3)A.滴加石蕊溶液,搅拌后溶液变蓝,说明氢氧化钠溶液过量;
B.滴加氢氧化钠溶液,搅拌后溶液颜色不变,说明加入的氢氧化钠和稀盐酸发生了反应,进一步说明稀盐酸过量;
C.加入蒸馏水,搅拌后溶液颜色不变,不能说明稀盐酸过量;
D.加入金属Zn片,产生气泡,说明稀盐酸过量.
故填:BD.
(4)①如图“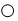 ”中填写的离子符号是H+.
”中填写的离子符号是H+.
故填:H+.
②从微观角度分析可知,氢离子和氢氧根离子结合生成了水分子,因此该反应的实质是氢离子和氢氧根离子结合生成水分子.
故填:氢离子和氢氧根离子结合生成水分子.
(5)①在“步骤一”中有计算、称量、溶解三个具体步骤.
故填:称量.
②在往稀盐酸中逐渐滴入氢氧化钠溶液的过程中,在a点时稀盐酸过量,溶液中的微粒有H2O、H+、Na+、Cl-.
故填:H2O、H+、Na+、Cl-.
③I.设稀盐酸中氯化氢质量为x,恰好完全反应时生成氯化钠质量为y,
NaOH+HCl═NaCl+H2O,
40 36.5 58.5
16g×1% x y
$\frac{40}{16g×1%}$=$\frac{36.5}{x}$=$\frac{58.5}{y}$,
x=0.146g,y=0.234g,
该稀盐酸的溶质质量分数为:$\frac{0.146g}{10g}$×100%=1.46%,
答:稀盐酸的质量分数是1.46%.
II.b点时溶液中溶质的质量分数为:$\frac{0.234g}{10g+16g}$×100%=0.9%,
答:b点时溶液中溶质的质量分数为0.9%.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


科目:初中化学 来源: 题型:多选题
| A. | KNO3晶体(NaCl):将固体溶于水配制成热的饱和溶液,采用降温结晶的方法 | |
| B. | FeSO4溶液(CuSO4):加入铁粉,过滤 | |
| C. | MnO2固体 (KCl):加足量水溶解,过滤、洗涤,干燥 | |
| D. | O2(N2):将混合气体通过炽热的铜网 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 地球上的水储量是丰富的,但是可利用的淡水资源是有限的 | |
| B. | 实验室用的蒸馏水是净化程度较高的水 | |
| C. | 用肥皂水可区分硬水和软水 | |
| D. | 硬水经过过滤后就能变成软水 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 如图是同学们探究过的三个重要实验,仔细观察,回答下列问题:
如图是同学们探究过的三个重要实验,仔细观察,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com