
 如图所示,图1为电解水的装置,图2为电解水生成的气体体积与时间的关系图.若甲管生成气体M,下列说法正确的是 ( )
如图所示,图1为电解水的装置,图2为电解水生成的气体体积与时间的关系图.若甲管生成气体M,下列说法正确的是 ( )| A. | b应接电源负极 | |
| B. | 气体N是氧气,气体M是氢气 | |
| C. | 用带火星的木条检验气体M,带火星的木条复燃 | |
| D. | 8min时,M、N的质量比为1:2 |
分析 根据电解水的实验现象及结论可以完成该题的解答,对于现象可以用六个字来概括:正氧一,负氢二,同时通过该实验能够得出在水中含有氢氧两种元素,可以据此答题.
解答 解:A、由电解水生成的气体体积与时间的关系可知,甲中生成的气体M较较多是氢气,乙中生成的气体N较少是氧气,b应接电源正极,故A错误;
B、由上分析可知,气体N是氧气,气体M是氢气;故B正确;
C、由上述分析可知,气体M是氢气,不具有助燃性,不能使带火星的木条复燃,故C错误;
D、根据电解水生成的气体体积与时间的关系可知,8min时,M、N的体积比为2:1;故D错误.
故选:B.
点评 熟记电解水的实验现象和结论,能够根据图象得出电源的正负极,并根据生成了氧气和氢气来判断水的组成元素.


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 步骤 | 实验操作 | 实验现象 | 实验结论 |
| 1 | 向试管中加入5mL浓硫酸,将铜丝伸入浓硫酸中,给试管加热. | 有白色固体出现,产生气泡 | |
| 2 | 用燃着的木条引燃产生的气体 | 未听见爆鸣声 | 猜想一不成立. (填“成立”或“不成立”) |
| 3 | 猜想二成立 |
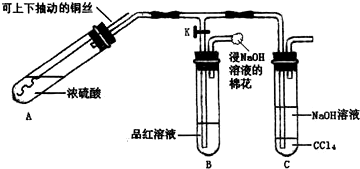
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
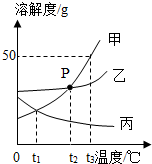 如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题.
如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图为某分子的结构模型,请回答下列问题:
如图为某分子的结构模型,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
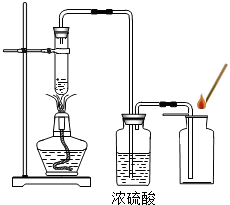 某学校化学兴趣小组同学在学习了制取氧气这一节内容后,发现在实验室里用5%H2O2溶液加热制O2,用带火星的木条检验,木条很难复燃.
某学校化学兴趣小组同学在学习了制取氧气这一节内容后,发现在实验室里用5%H2O2溶液加热制O2,用带火星的木条检验,木条很难复燃.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | (1)(2)(5) | B. | (1)(3)(6) | C. | (1)(4)(5) | D. | (1)(2)(6) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com