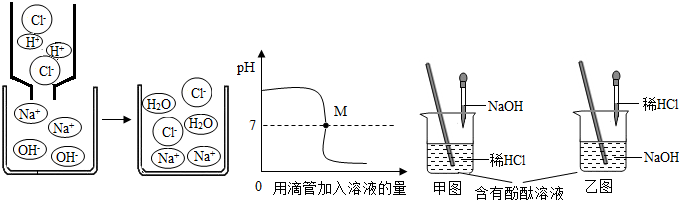
中和反应在日常生活和工农业生产中有广泛应用.如:
(1)农业上可用来降低土壤的酸性,改良土壤结构的物质是 ______.
(2)医疗上可用含氢氧化镁的药物来中和过多的胃酸(视为盐酸),有关反应的化学方程式为 ______.
(3)如何检验某硫酸厂排出的废水是否具有酸性?请设计出两种实验方案(写出简要的实验步骤、现象及结论).
方案一:______;
方案二:______.
(4)取某硫酸厂排出的一定体积的废水与一定量的氢氧化钠溶液混合后,溶液恰好呈中性.若改用与该氢氧化钠溶液的质量和溶质质量分数均相同的氢氧化钾溶液与上述一定体积的废水混合,则所得溶液的pH ______7(填“>”、“<”或“=”).
【答案】分析:氢氧化钙具有碱性,可以用来改良酸性土壤,胃液中含有的酸为盐酸,可以用碱性物质中和过多的盐酸,检验物质的酸性,可以使用酸碱指示剂石蕊,观察其颜色变化,也可以与碳酸盐混合观察有无气泡产生,改用氢氧化钾与硫酸反应要判断溶液的酸碱性需经过计算.
解答:解:(1)常用来改良酸性土壤的物质是氢氧化钙,所以本题答案为:Ca(OH)2;
(2)氢氧化镁可以与胃液中的盐酸反应生成氯化镁和水,所以本题答案为:Mg(OH)2+2HCl═MgCl2+2H2O;
(3)酸性溶液能使石蕊变红,能与碳酸盐反应产生气体,所以本题答案为:
方案一:取少量该溶液置于试管中,向其中滴加几滴紫色石蕊试液,若变红,则证明废水具有酸性.
方案二:取少量该溶液置于试管中,向其中滴加几滴Na2CO3溶液,若有气泡产生,则证明废水具有酸性.
(4)2NaOH+H2SO4=Na2SO4+2H2O
80 98
若改成相同质量的氢氧化钾,则有
2KOH+H2SO4=K2SO4+2H2O
112 98
可以看出消耗相同质量的硫酸,需要氢氧化钾的质量多,故硫酸有剩余,溶液呈酸性,所以其PH小于7,所以本题答案为:
pH<7.
点评:本题考查了中和反应的应用,完成此题,可以依据已有的知识进行,在设计实验证明溶液的酸性时,可以根据酸的性质着手设计,本题的易错点是由氢氧化钠改用氢氧化钾与硫酸反应后溶液酸碱性的判断.



 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案