
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 加入氯化钙溶液质量/g | 20.0 | 60.0 | 80.0 |
| 生成沉淀质量/g | 1.0 | m | 3.5 |
分析 (1)根据第一次实验数据可知,每消耗20.0g氯化钙溶液,生成沉淀质量1.0g,所以假设第二次60.0g氯化钙溶液完全反应,生成沉淀质量沉淀为3.0g<3.5g,说明第二次60.0g氯化钙溶液完全反应;第三次加入80.0g氯化钙溶液,只生产沉淀质量沉淀为3.5g,说明氯化钙溶液过量,碳酸钠完全反应.
(2)据生成沉淀碳酸钙的质量可计算样品中所含碳酸钠的质量,则氢氧化钠的质量=13.5g-碳酸钠的质量,进一步求解样品中含氢氧化钠的质量分数,据此解答即可;
(3)由于第一、二次实验中氯化钡完全反应,计算氯化钙溶液的质量分数,按第一、二次实验进行,据生成沉淀碳酸钙的质量可计算样品中所含氯化钡的质量,进一步求解氯化钙溶液的质量分数.
解答 解:(1)第一次实验数据可知,每消耗20.0g氯化钙溶液,生成沉淀质量1.0g,所以假设第二次60.0g氯化钙溶液完全反应,生成沉淀质量沉淀为3.0g<3.5g,说明第二次60.0g氯化钙溶液完全反应,所以m=3.0;
(2)设恰好完全反应时参加反应的碳酸钠的质量为x,
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 3.5g
$\frac{106}{x}=\frac{100}{3.5g}$
x=3.71g
样品中含氢氧化钠的质量分数为$\frac{13.5g-3.71g}{13.5g}×100%$=72.5%;
(3)设第一次参加反应的氯化钡的质量为y
Na2CO3+CaCl2═CaCO3↓+2NaCl
111 100
y 1.0g
$\frac{111}{y}=\frac{100}{1.0g}$
y=1.11g
反应前滴加氯化钙溶液的质量分数$\frac{1.11g}{20g}×100%$=5.55%;
故答案为:(1)3.0;
(2)72.5%;
(3)5.55%.
点评 本题主要考查学生运用化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.


科目:初中化学 来源: 题型:选择题
| A. | Ca+、Cu2+、NO3-、Cl- | B. | Na+、Ag+、SO42-、Cl- | ||
| C. | Na+、Ba2+、Cl-、NO3- | D. | Na+、K+、CO32-、SO42- |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
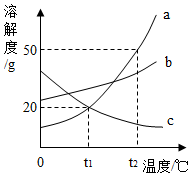 a、b、c三种固体物质的溶解度曲线如图所示,下列叙述正确的是( )
a、b、c三种固体物质的溶解度曲线如图所示,下列叙述正确的是( )| A. | a物质的溶解度大于b物质的溶解度 | |
| B. | t1℃时,a、c两种物质的溶液的质量分数相等 | |
| C. | t2℃时,30ga物质加入50g水中得到80g溶液 | |
| D. | t2℃时,a、b、c三种物质的饱和溶液降温到t1℃时所得溶液质量分数由大到小的顺序是b>a>c. |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | S02、CO、NO2都是造成空气污染的气体 | |
| B. | 喝汽水打嗝,是因为气体溶解度随温度升高而增大 | |
| C. | 燃烧需要同时满足三个条件,灭火只需要破坏至少一个条件即可 | |
| D. | 合金硬度一般比组成它的纯金属大 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤液中一定有氯化镁,可能有氯化锌和氯化亚铁 | |
| B. | 滤液中一定有氯化镁和氯化锌,可能有氯化铜 | |
| C. | 滤渣中一定有铜和铁,可能有锌 | |
| D. | 滤渣中一定有铜,可能有铁和锌 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com