
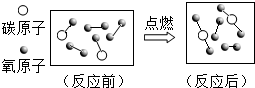
| ||
| ||


科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:

| 组别 | 样品质量 | CO2的体积 |
| 第1组 | 0.21g | 22.39mL |
| 第2组 | 0.21g | 22.41mL |
| 第3组 | 0.21g | 22.40mL |
查看答案和解析>>
科目:初中化学 来源: 题型:
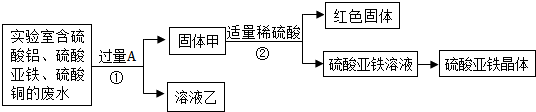
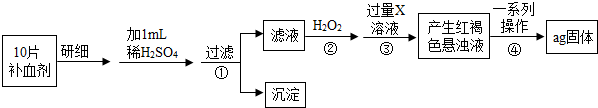
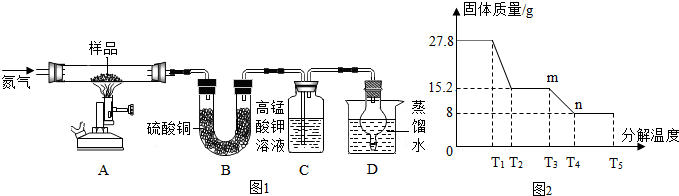
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
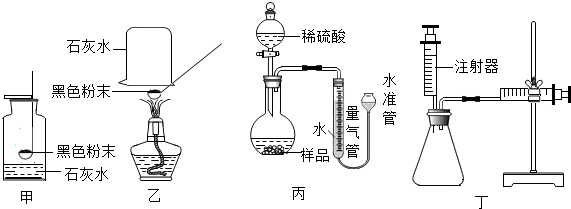
| 品名 | XX牌贴身暖宝宝 |
| 成分 | 带内物质:铁粉、水、活性炭、食盐等 |
| 内袋材料 | 微孔透气无纺布 |
| 外袋材料 | 不透气塑料 |
| 用法 | 临使用前,打开外袋取出内袋,直接贴在衣服上. 打开外袋后保持温暖12小时 |
| 实验操作 | 实验现象 | 解释或结论 | |
| 步骤1 | 取A、B两袋“暖宝宝”,将A袋按使用说明打开外袋取出内袋;而B袋不打开外袋.并将两袋样品放置在同样的环境中. | A袋的“暖宝宝”温度很快上升;B袋温度 | “暖宝宝”发热是由于袋内物质与 |
| 步骤2 | 24小时后,分别剪开A、B两袋,各取少量袋内物质于两支试管中,分别加入适量稀盐酸. | A袋内物质部分溶解,产生黄色溶液;B袋内物质 | 用化学方程式表示产生黄色溶液的反应 |
| 得出结论】“暖宝宝”发出的热量主要来自铁粉发生氧化(生锈)的过程. | |||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
 碳元素是组成许多物质的基本元素.
碳元素是组成许多物质的基本元素.查看答案和解析>>
科目:初中化学 来源: 题型:
| 收费项目 | 单位(元/立方米) | 应收金额(元) |
| 自来水水费 | 1.70 | 15.30 |
| 水资源费 | 1.26 | 11.34 |
| 污水处理费 | 1.04 | 9.36 |
| 合计金额 | / | 36.00 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com