
【题目】如图所示是全球最大太阳能飞机“阳光动力2号”。
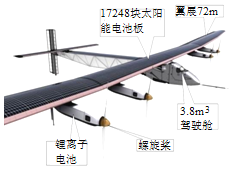
“阳光动力2号”的机身和机翼均采用碳纤维复合材料制成,该机的机翼、机身和水平尾翼上共贴敷了17248 片135pμm厚的单晶硅薄膜太阳能电池。请回答下列问题:
(1)碳纤维复合材料是有机纤维经过一系列热处理转化而成,含碳量高于90%,其强度比钢高五倍,重量却不到钢的一半。碳纤维复合材料具有的优良性能是________(填字母)。
A 硬度大、密度大
B 密度小、熔点低
C 密度小、强度高
(2)太阳能电池芯片的常用材料是“单晶硅”。硅的元素符号是①_______,高纯硅常用作半导体材料,这说明硅具有②_________性。
(3)制造该飞机时常用乙炔( C2H2)进行焊接。实验室可以用电石( CaC2 )和水反应制得乙炔气体,同时生成一种碱。该反应的化学方程式为①__________,电石中碳元素的化合价是②________。
(4)太阳能飞机与用航空煤油做燃料的飞机相比,不仅可以节约_______,还可以减少对空气的污染。
【答案】C Si 导电 ![]() -1 价 石油资源
-1 价 石油资源
【解析】
(1)碳纤维复合材料的强度比钢高五倍,说明强度高;其重量却不到钢的一半,说明密度小。因此碳纤维复合材料具有的优良性能是密度小、强度高,故选C。
(2)硅的元素符号是Si,书写时要注意第一个字母大写,第二个字母小写;高纯硅常用作半导体材料,这说明硅具有导电性。
(3)电石(CaC2)和水反应制得乙炔(C2H2)气体,根据质量守恒定律和碱的组成可知,生成的一种碱是Ca(OH)2。该反应的化学方程式为![]() ,已知电石的化学式为CaC2,钙元素化合价为+2价,根据化合物元素化合价代数和为零,设碳元素化合价为x,则
,已知电石的化学式为CaC2,钙元素化合价为+2价,根据化合物元素化合价代数和为零,设碳元素化合价为x,则![]() ,x=-1,电石中碳元素的化合价是-1 价。
,x=-1,电石中碳元素的化合价是-1 价。
(4)太阳能飞机与用航空煤油做燃料的飞机相比,不仅可以节约石油资源,还可以减少对空气的污染。


科目:初中化学 来源: 题型:
【题目】黄铜是铜和锌的合金。某化学兴趣小组的同学欲测定某黄铜样品中铜的质量分数(不考虑黄铜中的其他杂质),请你参与他们的探究过程。称量10g粉末状黄铜样品放入烧杯中,把60g某浓度的稀硫酸分三次加到其中,每次充分反应后,测定生成氢气的质量,实验数据如下表:
第一次 | 第二次 | 第三次 | |
加入稀硫酸的质量(g) | 20 | 20 | 20 |
生成氢气的质量(g) | 0.04 | m | 0.02 |
试求:
(1)m的数值________。
(2)60g该硫酸溶液的溶质质量分数是_______?(写出计算过程,计算结果保留1位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组对氧气的制取和性质实验进行探究。
(1)现有如下装置:

①实验室用氯酸钾和二氧化锰制氧气的化学方程式为_____________,应选择的发生装置和收集装置是____________。
②用收集到的氧气进行“硫在氧气中燃烧”的实验,观察到的现象是 ______________。
(2)氯化氢和氨气发生了化学反应,可生成氯化铵白色固体。 某兴趣小组利用浓氨水和浓盐酸探究分子运动速度与相对分子质量的关系。
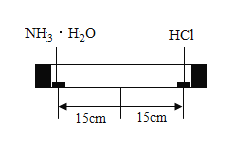
(实验方案)将一支约 40 cm 长的玻璃管水平放置,向左、右两端的玻璃管口分别同时滴入等量的浓氨水和浓盐酸,塞紧橡皮塞。 过一会儿后,观察到有白烟产生且位置偏右。
(实验结论)上述实验说明:① ________________。
②分子的运动速率与相对分子质量有关,其关系是____________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国药学科学家屠呦呦创制新型抗疟药﹣﹣青蒿素(C15H22O5)和双氢青蒿素,因此而获得2015年诺贝尔医学奖。计算:
(1)青蒿素(C15H22O5)的相对分子质量为_____;
(2)青蒿素(C15H22O5)中碳、氢、氧三种元素质量比为_____(填最简比);
(3)青蒿素(C15H22O5)中碳元素的质量分数为_____(精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某学习小组的同学们在学习了酸、碱盐的相关性质后,做了如下实验,请与他们一起探究:

甲同学实验时发生反应的化学方程式为__________。
乙同学观察到的实验现象为____________。
实验结束后,甲、乙同学将试管中清液倒入同一烧杯中,发现产生白色沉淀,由此可知乙同学实验所得溶液中含有的溶质是_________(填化学式)。
[提出问题]烧杯内滤液中含有哪些离子呢?
同学们将烧杯中固液混合物分离,取滤液少许,向其中加入过量的碳酸钠溶液,无明显现象。
[假设与猜想]甲同学:Na+、Cl-
乙同学:Na+、Cl-、OH-
丙同学:Na+、Cl-、SO42-、Ba2+
[表达与交流]大家一致认为___________同学的猜想是错误的。理由是________。
[活动与探究]甲同学为了验证自己的猜想,取烧杯中滤液少许,加入无色酚酞溶液,没有观察到明显实验现象,于是认为自己的猜想正确。大家都认为甲同学的实验结论_______ (填“正确”或“不正确”)。同学们通过实验最终确定了滤液中的离子成分。
[反思与收获]由上述探究活动可知,当溶液中待测离子较多时,可以先加入试剂,根据_______排除一些猜想。当溶质组成只剩两种情况时,加人适当的试剂,证明______即可。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是从微观角度研究物质的组成、结构及变化的科学,构成物质的粒子之间的关系如图1所示,请回答下列问题:

(1)甲是_____.
(2)氢气、金刚石、硫酸铜三种物质中,由离子构成的物质是_____.
(3)图2是氟元素的原子结构示意图,方框横线上的数字是______.
(4)在化学变化前后一定发生改变的是______(填字母).
A 元素的种类 B 原子的个数 C 原子的质量 D 分子的种类
(5)氟元素和氢元素形成的化合物的水溶液叫氢氟酸(HF),可用于雕刻玻璃,其主要原因是氢氟酸和玻璃的主要成分二氧化硅发生反应,生成四氧化硅气体和水,写出该反应的化学方程式_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验现象描述错误的是( )
A.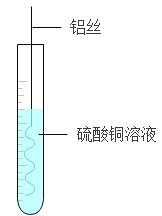 铝丝浸入硫酸铜溶液中:银白色固体表面覆盖一层紫红色固体,蓝色溶液逐渐变为无色
铝丝浸入硫酸铜溶液中:银白色固体表面覆盖一层紫红色固体,蓝色溶液逐渐变为无色
B. 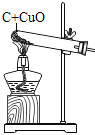 木炭还原氧化铜:黑色粉末逐渐变为紫红色
木炭还原氧化铜:黑色粉末逐渐变为紫红色
C.  镁条燃烧:银白色固体燃烧,发出耀眼的白光,放热,产生白烟,生成白色固体
镁条燃烧:银白色固体燃烧,发出耀眼的白光,放热,产生白烟,生成白色固体
D.  焚烧含氯塑料:产生有刺激性气味的氯化氢气体
焚烧含氯塑料:产生有刺激性气味的氯化氢气体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)为测定某赤铁矿石中氧化铁的质量分数,小龙和他的同学用跑题的一氧化碳与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用一定量的氢氧化钠溶液完全吸收,该溶液总质量与反应时间的变化关系如图。

(1)上述反应产生二氧化碳的质量为 g;
(2)计算该赤铁矿石中氧化铁的质量分数;
⑶若上述反应后剩余固体质量为m克,写出计算该赤铁矿石中氧化铁质量分数的表达式: (用m表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com