
在元素周期表中,硫元素的信息如图所示,下列从图中获得的信息不正确的是( )

A.在硫原子的核外电子排布中a=2和b=8
B.硫原子在化学反应中易获得2个电子生成S2﹣
C.硫原子里,质子数=中子数=电子数=16
D.一个硫原子的相对原子质量是32.06克
【分析】A、根据原子核外第一层上有2个电子、第二层上有8个电子,进行分析判断.
B、若原子的最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子.
C、左上角的数字表示原子序数,汉字下面的数字表示相对原子质量,进行分析判断即可.
D、汉字下面的数字表示相对原子质量,据此进行分析判断.
【解答】解:A、原子核外第一层上有2个电子、第二层上有8个电子,在硫原子的核外电子排布中a=2和b=8,故选项说法正确.
B、硫原子的最外层电子数是6,大于4,在化学反应中易得到2个电子而形成S2﹣,故选项说法正确.
C、根据元素周期表中的一格可知,左上角的数字为16,表示原子序数为16;根据原子序数=核电荷数=质子数=核外电子数,则该 元素的原子核内质子数和核外电子数均为16;汉字下面的数字表示相对原子质量,硫元素的相对原子质量为32.06≈32,相对原子质量=质子数+中子数,则中子数=32﹣16=16,故选项说法正确.
元素的原子核内质子数和核外电子数均为16;汉字下面的数字表示相对原子质量,硫元素的相对原子质量为32.06≈32,相对原子质量=质子数+中子数,则中子数=32﹣16=16,故选项说法正确.
D、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,硫元素的相对原子质量为32.06,相对原子质量单位是“1”,不是“克”,故选项说法错误.
故选:D.


科目:初中化学 来源: 题型:
溶液是自然界中常见的物质.下列有关溶液的说法正确的是( )
A.溶液的上层浓度小,下层浓度大
B.溶液蒸干后,均能得到固体溶质
C.溶液中只有一种溶质时,溶液为纯净物
D.物质在溶解得到溶液的过程中,通常有放热或吸热的现象出现
查看答案和解析>>
科目:初中化学 来源: 题型:
如图中A、B、C、D是四种粒子的结构示意图.请回答下列问题:
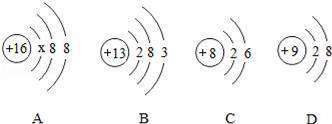

(1)A中x= ;A粒子的化学式是 .
(2)由B粒子的结构示意图可知,B粒子的名称是 .
(3)以上四种结构示意图所表示的粒子中,表示离子的是 (填字母代号).
查看答案和解析>>
科目:初中化学 来源: 题型:
下列除杂(括号内为杂质)选用的试剂或方法正确的是( )
A.CuO(C):隔绝空气高温加热
B.CaCl2溶液(HCl):加入过量碳酸钙,充分反应后过滤
C.CO2(CO):点燃
D.BaSO4(BaCO3):加足量稀盐酸、过滤、蒸发、结晶
查看答案和解析>>
科目:初中化学 来源: 题型:
工业上用电解饱和NaCl溶液的方法来制取NaOH、Cl2和H2,并以它们为原料生产一系列化工产品,称为氯碱工业.在工业上,制取氯气和烧碱的主要工艺流程如下:

环节Ⅰ:利用海水提取粗盐的过程(如图).

(1)图中①是 (填“蒸发”或“冷却”)池.
(2)母液为氯化钠的 (填“饱和”或“不饱和”)溶液.
环节Ⅱ:利用工业上粗盐(含MgCl2、CaCl2、Na2SO4等杂质)精制氯化钠(工艺流程如图).

(1)X中含有的阳离子是 ;
(2)写出生成沉淀D的一个化学方程式 .
(3)溶液E中加过量稀盐酸的作用是 .
(4)实验所得精盐的质量大于粗盐中NaCl的质量,原因是 .
环节Ⅲ:电解饱和食盐水生产氯气和烧碱并测定烧碱的纯度.
(1)请写出环节Ⅲ生产中发生反应的化学方程式 .
(2)工业烧碱常常含有一定的氯化钠和碳酸钠杂质.为了测定烧碱的含量,小婉同学设计探究方案后进行实验并测得数据如图:

请你利用小婉同学测得的数据计算烧碱样品中氢氧化钠的质量分数(请列出计算过程) .
(3)小强同学认为小婉同学设计的探究方案不够严密,其理由是:
①探究方案中没考虑氢氧化钠的吸水性.
②探究方案中因缺少 (填操作名称),导致测得的氢氧化钠的质量分数偏小.
环节Ⅳ:应用举例
氯气与氢氧化钠溶液反应的化学方程式为:Cl2+2NaOH═NaCl+NaClO+H2O,工业上用氯气与石灰乳[Ca(OH)2]反应来制取漂白粉,有关反应的化学方程式是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
下列关于物质的性质和用途说法不正确的是
A.氮气充入食品中防腐,是利用氮气常温下化学性质稳定
B.氧气用于火箭发射,是利用氧气的可燃性
C.制作霓虹灯时充入稀有气体,是利用稀有气体通电能发出不同颜色的光
D.氦气可用来填充探空气球,是利用氦气的密度小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com