
| 98 |
| x |
| 80 |
| 1.6g |
| 1.96g |
| 10g |


科目:初中化学 来源: 题型:
| A、76 | B、86 | C、136 | D、96 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取一瓶呼出气体和等体积的一瓶空气,将燃着的小木条分别同时伸入瓶中,盖上玻璃片 | 人体呼出气体中氧气的含量比空气中氧气的含量少 | |
| (2) |
人体呼出的气体中水蒸气的含量比空气中水蒸气的含量多 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生产生O2体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |
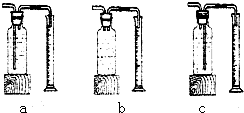
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com