


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:初中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
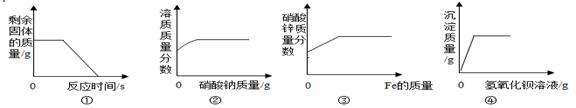
| A.图①是将一定质量的碳酸钙充分煅烧 |
| B.图②是在一定温度下,向不饱和硝酸钠溶液中不断加入硝酸钠固体,充分搅拌 |
| C.图③是向一定质量的Zn(NO3)2和Cu(NO3)2的混合溶液中不断加入铁粉 |
| D.图④是向Na2SO4和HCl的混合溶液中不断滴入氢氧化钡溶液 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题


查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.Mn+H2SO4=MnSO4+H2↑ | B. Mg+MnCl2=MgCl2+Mn |
| C.Fe+MnCl2=FeCl2+Mn | D. Mn+CuCl2=MnCl2+Cu |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
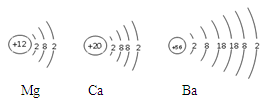
| A.Mg>R>Cu | B.Cu>R>Mg | C.R>Mg>Cu | D.Mg>Cu>R |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.①② | B.①②③ | C.③④ | D.①②④ |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验步骤 | 现象 | 结论 |
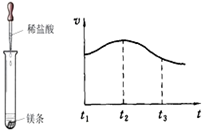
| (1)取少量红色固体于一支洁净的试管中,加入稀盐酸 | __________________________________ | 猜想一不成立 |
| (2)①用尖嘴导管将气体导出并引燃,同时在上方放一块干冷的玻璃片 ②取少量红色固体于一支洁净的试管中,加入稀硝酸 | 该气体能燃烧,且玻璃片上有______出现 红色固体溶解,得到蓝色溶液同时看到试管上部有红棕色气体产生 | 猜想二成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com