
分析 (1)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
(2)根据化学方程式和大理石的质量、纯度,计算生成二氧化碳的质量;
(3)根据化学方程式和大理石的质量、纯度,计算参加反应的稀盐酸的质量;
(4)根据溶液稀释前后,溶质质量不变进行分析;
(5)根据大理石中钙元素的质量和损耗的质量分数,依据钙元素守恒计算生成氯化钙的质量.
解答 解:(1)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)设可制得二氧化碳的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
25g×80% x
$\frac{100}{25g×80%}$=$\frac{44}{x}$
(3)设需要盐酸的质量为y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73
25g×80% y×7.3%
$\frac{100}{25g×80%}$=$\frac{73}{y×7.3%}$
y=200g
(4)需要浓盐酸的质量为:$\frac{200g×7.3%}{36.5%}$=40g,所以需浓盐酸和水的质量比为40g:(200g-40g)=1:4;
(5)大理石中含有钙元素的质量为:250g×80%×$\frac{40}{100}$=80g,参加反应的钙元素质量为:80g×(1-20%)=64g,所以生成氯化钙的质量为:$\frac{64g}{\frac{40}{111}×100%}$=177.6g,所以最后可得40%的氯化钙溶液的质量为$\frac{177.6g}{40%}$=
444g.
故答案为:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)$\frac{100}{25g×80%}$=$\frac{44}{x}$;
(3)200g;
(4)1:4;
(5)444g.
点评 本题可很好考查学生分析、解决问题的能力,计算较多,要找准已知量,细心分析.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:初中化学 来源: 题型:实验探究题
 有一包白色固体可能含碳酸钠、硫酸钠、氯化钾、硝酸钡中的一种或几种.某化学兴趣小组为探究其成分进行了以下实验:
有一包白色固体可能含碳酸钠、硫酸钠、氯化钾、硝酸钡中的一种或几种.某化学兴趣小组为探究其成分进行了以下实验:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用托盘天平称取了6.8gNaCl | |
| B. | 用pH试纸测得某溶液酸碱度为7.5 | |
| C. | 用量筒量取了15.67mL水 | |
| D. | 常温下,M的溶解度为36g,可配得该温度下36%的M溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
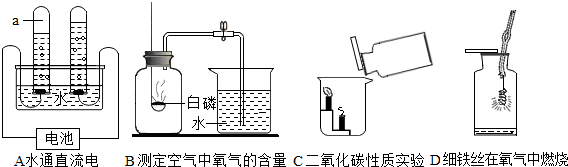
| 铁丝中含碳量 | 0.05% | 0.2% | 0.6% |
| 燃烧时的现象 | 剧烈燃烧,极少火星 | 剧烈燃烧,少量火星 | 剧烈燃烧,大量火星 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
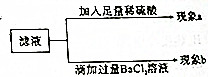 在做课本纯碱的化学性质分组实验时,第-组学生进行Na2CO3与BaC12溶液的反应,第二组学生进行Na2CO3与H2SO4溶液的反应.
在做课本纯碱的化学性质分组实验时,第-组学生进行Na2CO3与BaC12溶液的反应,第二组学生进行Na2CO3与H2SO4溶液的反应.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用硫酸铜溶液鉴别氢氧化钠和碳酸钠溶液 | |
| B. | 用紫色石蕊试液测定雨水的酸碱度 | |
| C. | 往固体中加入稀盐酸,出现气泡说明该固体一定是碳酸盐 | |
| D. | 只用酚酞试液就能将氯化钠溶液、氢氧化钠溶液、盐酸区别开来 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com