
| A. | 锌一定有剩余 | B. | 硫酸一定有剩余 | ||
| C. | m值大于或等于5.6 | D. | 可以确定稀硫酸浓度为19.6% |
分析 根据等质量铁和锌与足量的稀硫酸反应,铁放出氢气的质量大于锌,而题设中产生氢气量均为0.2g,可推断出稀硫酸量不足而被完全反应,而金属铁一定有剩余;
假设锌与硫酸恰好完全反应,根据生成氢气的质量可计算出金属质量m的最小值及参加反应的硫酸的质量,利用稀硫酸的质量分数=$\frac{参加反应的硫酸质量}{稀硫酸质量50g}$×100%可计算该稀硫酸中溶质的质量分数进行分析.
解答 解:根据反应的化学方程式可得知,等质量铁和锌与足量的稀硫酸反应,铁放出氢气的质量大于锌;由“质量分数相同的稀硫酸”、“充分反应后均产生0.2g氢气”可知,稀硫酸完全反应,故B错误;产生等质量的氢气,消耗的铁的质量小于消耗的锌的质量,由于充分反应产生等质量的氢气,可判断金属铁一定有剩余、锌可能有剩余或恰好完全反应,故A错误;
假设锌恰好完全反应,根据反应的化学方程式,
Zn+H2SO4═ZnSO4+H2↑
65 98 2
6.5g 9.8g 0.2g
产生0.2g氢气可计算至少需要6.5g锌,m的值等于6.5g时锌无剩余,大于6.5g时有剩余,故C错误;
需要9.8gH2SO4,可计算出溶质的质量分数=$\frac{9.8g}{50g}$×100%=19.6%,故D正确.
故选:D.
点评 对于金属与足量的酸反应放出氢气的量还可以通过以下算式计算与对比:放出氢气的质量=$\frac{金属化合价}{金属相对原子质量}$×金属质量.


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:初中化学 来源: 题型:解答题
| 烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ | |
| 加入样品的质量/g | 10 | 10 | 10 | 10 | 10 |
| 加入稀盐酸的质量/g | 10 | 20 | 30 | 40 | 50 |
| 充分反应后生成气体的质量/g | 0.88 | 1.76 | 2.64 | 3.52 | 3.52 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
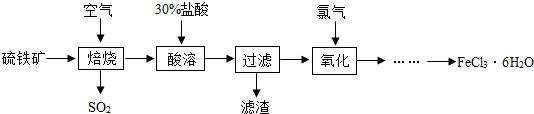
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
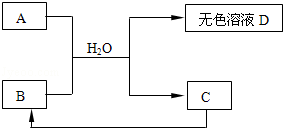
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
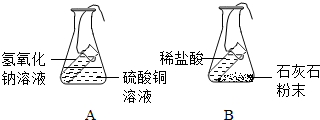 小明为了探究质量守恒定律,设计了A、B两个实验装置(如图所示).
小明为了探究质量守恒定律,设计了A、B两个实验装置(如图所示).查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 可吸入颗粒物 | 氮氧化合物 | 二氧化硫 | 空气质量级别 | |
| 春季 | 88 | 40 | 44 | Ⅱ |
| 夏季 | 67 | .33 | 36 | Ⅱ |
| 秋季 | 90 | 46 | 54 | Ⅱ |
| 冬季 | 98 | 69 | 60 | Ⅱ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铜在空气中受热:紫红色固体变成黑色 | |
| B. | 氢氧化铝能使紫色石蕊试液变蓝色 | |
| C. | 氢气在空气中燃烧:发蓝光,放热 | |
| D. | 木炭还原氧化铜:黑色固体中出现紫红色固体,生成二氧化碳气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com