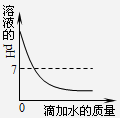
如图1像表示盐酸和氢氧化钠溶液发生反应过程中溶液的pH变化.请从图象中获取信息,回答下列问题:
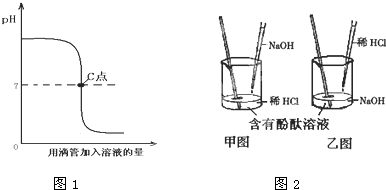
(1)进行该反应的实验操作是按照以上图2中
乙
乙
(填甲或乙)图所示进行,烧杯中溶液的颜色变化是
红色变为无色
红色变为无色
.
(2)曲线上C点表示
盐酸和氢氧化钠刚好完全中和
盐酸和氢氧化钠刚好完全中和
(3)用溶质的质量分数为36.5%的盐酸40g与足量氢氧化钠溶液恰好完全反应,需要溶质的质量分数为20%的氢氧化钠溶液
80
80
g.
(4)甲乙丙丁四位同学在氢氧化钠溶液滴入酚酞试液时,发现了一个意外现象:溶液变成了红色,一会儿红色就消失了.
【猜想】
甲:可能是酚酞变质的缘故;
乙:可能是氢氧化钠溶液与空气中二氧化碳反应的缘故;
丙:可能是酚酞与空气中氧气反应,使红色消失的缘故;
丁:可能与氢氧化钠溶液质量分数大小有关.
【查阅资料】
碳酸钠溶液显碱性.
【理论分析】
甲同学刚提出自己的猜想,就遭到其余三位同学的否定,三位同学的理由是
氢氧化钠溶液滴入酚酞试液,溶液变成了红色,可排除酚酞变质
氢氧化钠溶液滴入酚酞试液,溶液变成了红色,可排除酚酞变质
. 乙同学的猜想也不正确,理由是
碳酸钠溶液显碱性,也可使酚酞试剂变红
碳酸钠溶液显碱性,也可使酚酞试剂变红
.
【实验设计】
为证实丙同学的猜想,还需作如下实验,请完成下表.
| 实验步骤 |
设计这一步骤的目的 |
| 1、用煮沸过的蒸馏水配制氢氧化钠溶液 |
排出水中的氧气 |
| 2、在氢氧化钠溶液中滴入酚酞,并在上方滴一些植物油 |
隔绝空气 隔绝空气 |
(5)通过以上实验,四位同学看到:溶液先变成红色,一会红色消失.因此酚酞红色褪去与氧气无关.若丁同学的猜想正确,设计如下实验证明并完成有关问题
| 试验方法 |
观察到的现象和结论 |
| 方案一:分别配制不同质量分数的氢氧化钠溶液,然后各滴加2滴酚酞试液 |
质量分数小的溶液中红色不消失,质量分数大的溶液中红色消失,则证明 红色消失与氢氧化钠溶液质量分数大小有关 红色消失与氢氧化钠溶液质量分数大小有关 . |
| 方案二:将滴有酚酞试液的浓氢氧化钠溶液 加水稀释 加水稀释 |
溶液变红 溶液变红 |