
| 实验操作 | 实验现象 | 实验结论 |
| 取一定量纯碱样品配成溶液后,滴加过量的CaCl2溶液. | 产生白色沉淀 | 反应的化学方程式: Na2CO3+CaCl2═CaCO3↓+2NaCl |
分析 (1)碳酸钠和氯化钙反应生成白色沉淀碳酸钙和氯化钠;
(2)滴加的CaCl2溶液过量能使碳酸钠完全反应;
(3)如果不洗涤沉淀物时,由于沉淀物上附着有杂质,会导致测定的沉淀物质量偏大;
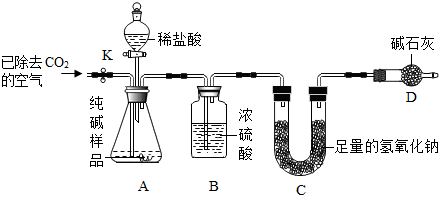
(4)打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的二氧化碳;
(5)碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳;
(6)根据质量守恒定律,装置C在反应前后的质量差就是产生CO2的质量;
若没有装置D,空气中的二氧化碳会进入装置C中.
解答 解:(1)取一定量纯碱样品配成溶液后,滴加过量的CaCl2溶液,产生白色沉淀,这是因为碳酸钠和氯化钙反应生成白色沉淀碳酸钙和氯化钠,反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl,实验过程如下表所示:
| 实验操作 | 实验现象 | 实验结论 |
| 取一定量纯碱样品配成溶液后,滴加过量的CaCl2溶液. | 产生白色沉淀 | 反应的化学方程式:Na2CO3+CaCl2═CaCO3↓+2NaCl |
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 该物质的化学式可能为C2H6O | |
| B. | 该物质的分子中碳原子与氢原子的个数比为1:2 | |
| C. | 该物质只含有碳元素和氢元素 | |
| D. | 该物质中碳元素与氢元素的质量比为12:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
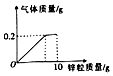 向盛有100g稀硫酸的烧杯中逐渐加入10g锌粒,产生气体质量与锌粒质量的关系如图所示.请根据关系图分析并计算:
向盛有100g稀硫酸的烧杯中逐渐加入10g锌粒,产生气体质量与锌粒质量的关系如图所示.请根据关系图分析并计算:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 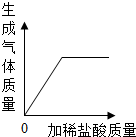 表示向部分变质的NaOH溶液中滴加稀盐酸至过量 表示向部分变质的NaOH溶液中滴加稀盐酸至过量 | |
| B. | 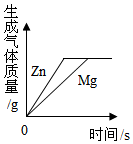 表示向溶质质量分数相同、等质量的稀硫酸中分别加入足量的金属镁和锌 表示向溶质质量分数相同、等质量的稀硫酸中分别加入足量的金属镁和锌 | |
| C. | 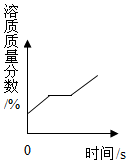 表示将一定质量的不饱和硝酸钾溶液恒温蒸发至有晶体析出 表示将一定质量的不饱和硝酸钾溶液恒温蒸发至有晶体析出 | |
| D. |  表示向一定量的盐酸和氯化钙溶液的混合物中不断滴入碳酸钠溶液 表示向一定量的盐酸和氯化钙溶液的混合物中不断滴入碳酸钠溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 住房着火,消防队员用水灭火,是为了降低可燃物的着火点 | |
| B. | 燃着的镁带在二氧化碳中会继续燃烧,因此镁等活泼金属着火不能用二氧化碳灭火 | |
| C. | 放在空气中的课本没有燃烧,是因为课本不是可燃物 | |
| D. | 油锅着火,用锅盖盖上,是为了降低可燃物的温度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com