
【题目】A~F六种物质共含H、C、O、N、Ca、Cu六种元素,分别为非金属单质、金属氧化物、非金属氧化物、酸、碱、盐中的一种。其中,A为温室气体,BC均为黑色固体,盐中不含金属。相邻物质之间能发生化学反应。

(1)A的固体俗称是_____,A与B的反应是_____反应(填“放热”或“吸热”)。
(2)E与F反应的现象是_____。
(3)C与D反应的化学方程式_____,属于_____反应(填基本反应类型)。
(4)除相邻物质之间能发生化学反应外,写出还能相互反应的化学方程式_____。
【答案】干冰 吸热 产生白色沉淀和有刺激性气味的气体 ![]() 复分解
复分解 ![]()
【解析】
A~F六种物质共含H、C、O、N、Ca、Cu六种元素,分别为非金属单质、金属氧化物、非金属氧化物、酸、碱、盐中的一种,A为温室气体,A为二氧化碳,属于非金属氧化物,A能B反应,B能与C反应,黑色的碳与二氧化碳地高温条件下生成一氧化碳,一氧化碳与黑色的氧化铜加热反应生成铜和二氧化碳,B、C均为黑色固体,则B为碳,属于非金属单质,C为氧化铜,属于金属氧化物,C能与D反应,硝酸能与氧化铜反应生成硝酸铜和水,则D是硝酸,属于酸, F能与A(二氧化碳)反应,氢氧化钙能与二氧化碳反应生成碳酸钙和水,F是氢氧化钙,属于碱,则E属于盐,盐中不含金属,E能D(硝酸)与反应,碳酸铵能与硝酸反应生成硝酸铵、水和二氧化碳,氢氧化钙能与碳酸铵反应生成碳酸钙、水和氨气,则E是碳酸铵,属于盐(碳酸铵由氮、氢、碳、氧元素组成,不含金属元素)。
(1)A为温室气体,A为二氧化碳,故A的固体俗称是干冰,A与B的反应是二氧化碳与碳在高温下反应生成一氧化碳,该反应是吸热反应。
(2)E与F反应是碳酸铵与氢氧化钙反应生成碳酸钙沉淀、氨气和水,故反应的现象是产生白色沉淀和有刺激性气味的气体。
(3)C与D反应是氧化铜能与硝酸反应生成硝酸铜和水,反应的化学方程式为![]() ,反应符合由两种化合物相互交换成分生成另外两种化合物,故属于复分解反应。
,反应符合由两种化合物相互交换成分生成另外两种化合物,故属于复分解反应。
(4)除相邻物质之间能发生化学反应外,还能相互反应的有氢氧化钙和硝酸反应生成硝酸钙和水,反应的化学方程式为![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】下列图像能正确反映对应的实验操作的是
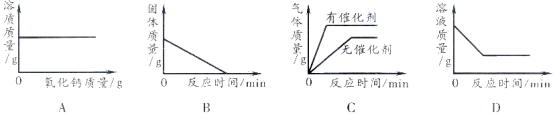
A.向一定量的饱和石灰水中加入氧化钙
B.加热一定量高锰酸钾固体产生氧气
C.用一定量的双氧水制取氧气
D.向一定量的硝酸银溶液中插入铜
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属材料广泛应用于生产生活中。
(1)常温下大多数金属是固体,但体温计中的金属是液体,该金属是________。用微粒的观点解释利用该金属应于体温的填充剂的原因:___________。
(2)贯休的《读唐史》中“洪炉烹五金,黄金终自奇”从金属的化学性质说明了金的化学性质是__________(填“活泼”或“不活泼”)。
(3)向含有氯化铜、氯化锌、稀盐酸的混合溶液中加入过量铁粉,充分反应后过滤,滤液中含有的溶质是_________(写化学式),试写出其中发生反应的化学方程式____________。
(4)用金属铁制备新型消毒、净水剂K2FeO4的流程图所示:
![]()
①步骤Ⅰ反应的发生反应的基本类型是___________。
②K2FeO4中Fe元素的化合价为_________。
③步骤Ⅱ发生得复分解反应的化学方程式为_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两小组同学分别用下图所示装置(夹持仪器已略去)做兴趣实验。
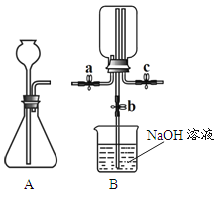
(1)甲组实验:
① 在A装置的锥形瓶中加入大理石,向长颈漏斗中注入稀盐酸,A中反应的化学方程式为_____。
② 连接A、B装置,打开a、c,关闭b,向B中集气瓶内充入气体,检验集气瓶中气体已收集满的方法是_____。
③ 关闭a、c,打开b,用冷毛巾捂住B中集气瓶,一段时间后,观察到B装置中的现象是_____, B中反应的化学方程式为_____。
(2)乙组实验:
【资料】氯化氢气体和氨气均极易溶于水,且两者反应生成白色固体氯化铵(NH4Cl)。
在c右端的导管口套一个气球,在A的锥形瓶中放入浓盐酸,向长颈漏斗中注入浓硫酸,有HCl气体产生,待A中的空气被排净后,连接A、B装置,打开a、c,关闭b,气球微微鼓起。产生HCl气体的原因是_____。
② 关闭a,将A中的药品替换为NaOH固体和浓氨水,待A中的空气被排净后,连接A、B装置,打开a,一段时间后关闭a,B中集气瓶内有白烟产生。冷却至室温后气球恢复原状。关闭c打开b,B中导管内的液面无任何变化。产生上述现象的原因是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用适当化学用语填空:
(1)3个亚铁离子_____;
(2)氦气_____;
(3)最简单的有机物_____;
(4)保持氧气的化学性质的微粒_____;
(5)标出纯碱中金属元素的化合价_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】亚硒酸钠(Na2SeO3)可用于提升人体免疫力,硒元素在元素周期表中的部分信息及原子结构示意图如图所示,下列说法正确的是( )

A.Na2SeO3中Se的化合价为+3 B.Se是一种金属元素
C.n的值为6 D.Se相对原子质量为78.96g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】研究元素知识是学好化学的基础,如表包含部分元素的相关信息,请完成填空。
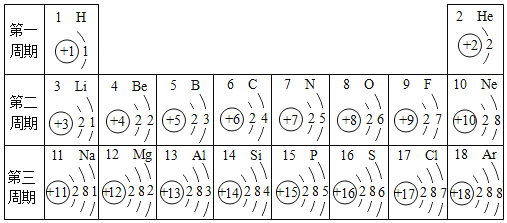
(1)1869年,俄国化学家_____发现了元素周期律并编制了元素周期表;
(2)用正确的化学用语填空:两个氢原子_____;2个氧分子_____;3个亚铁离子_____;氧化铝中铝元素显+3价_____
(3)下列图中微粒共表示_____种元素,其中与氯元素具有相似化学性质的是_____![]() 填序号
填序号![]() 。其中D元素位于第_____周期。
。其中D元素位于第_____周期。
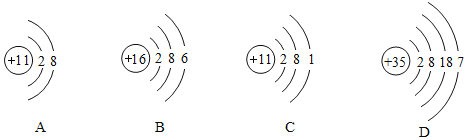
(4)写出原子序数为1、6、8、11四种元素所组成化合物的化学式_____。
(5)通过分析,同一横行元素之间的排列有一定的规律,如:①从左到右,由金属元素逐渐向非金属元素过渡;②从左到右,各元素原子的电子层数相同;③_____(任写一条)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工厂欲测定铝土矿中A12O3的含量,将矿石粉碎(其中杂质既不溶于水也不与酸反应),进行如下实验:
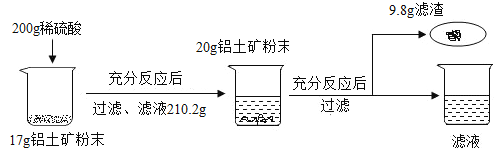
请回答下列问题:
(1)上述实验过程中发生反应的化学方程式为_____;
(2)铝土矿中A12O3的质量分数为_____;
(3)根据已知条件列出求解200g稀盐酸中溶质质量(X)的比例式_____;
(4)若将最终所得溶液蒸发掉20.4g水,所得不饱和溶液中溶质的质量分数为_____;
(5)用浓盐酸配置上述稀盐酸,需要的仪器有:烧杯、量筒、胶头滴管和_____;
(6)该炼铝厂每天用上述铝土矿170t来生产铝合金,则理论上日产含镁46%的铝镁合金的质量为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化钙应用广泛,以石灰石(杂质主要是Fe2O3、MgSO4)为原料生产氯化钙的流程如下。
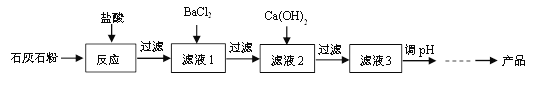
已知:BaCl2 + MgSO4 = BaSO4↓+ MgCl2
Ca(OH)2 + MgCl2 = Mg(OH)2↓+ CaCl2
Ca(OH)2 + FeCl3 = Fe(OH)3↓+ CaCl2
(1)氧化铁与盐酸反应的化学方程式为______。
(2)滤液1中的溶质有HCl、FeCl3、MgSO4和______。
(3)滤液2中加入Ca(OH)2是为了除去______(填序号,下同)。
A.MgCl2 B.FeCl3 C.HCl
(4)滤液3呈碱性,为使溶液pH降低,可加入适量的______。
A.NaCl B.NaOH C.盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com