

分析 (1)根据贝壳的主要成分分析即可;
(2)根据过滤操作的适用范围和所用到的仪器分析即可;
(3)根据元素守恒分析即可;
(4)根据氧化钙能与水反应生成氢氧化钙书写,
(5)根据氢氧化镁与盐酸的反应原理分析即可.
解答 解:(1)贝壳的主要成分是碳酸钙,化学式为:CaCO3;
(2)因为氢氧化镁为沉淀,不溶于水,所以可以通过过滤分离,过滤时需要的玻璃仪器有烧杯、玻璃棒、漏斗等;
(3)根据元素守恒可知产物还有氯气,故选:Cl2;
(4)第②步反应是氧化钙和水反应生成氢氧化钙,反应的化学方程式为CaO+H2O═Ca(OH)2;
(5)第③步反应是氢氧化镁与盐酸反应生成氯化钙和水,化学方程式为:Mg(OH)2+2HCl=MgCl2+2H2O.
故答案为:(1)CaCO3;
(2)漏斗;
(3)Cl2↑;
(4)CaO+H2O═Ca(OH)2;
(5)Mg(OH)2+2HCl=MgCl2+2H2O.
点评 本题考查了从海水中提取镁的原理和方法,从氯化镁中提取镁单质,应电解熔融态的氯化镁,而不能用置换的方法得到镁.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题


查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 浓硫酸(H2SO4)500毫升 | |
| 溶质的质量分数 | 98% |
| 密度 | 1.84克/厘米3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封储藏 | |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 生成物之一是H2O | B. | 该反应属于分解反应 | ||
| C. | 反应后催化剂质量增加 | D. | 反应前后分子数量不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 饱和溶液析出晶体后,溶质的质量分数可能不变 | |
| B. | “冬天捞碱,夏天晒盐”的主要原理是不同物质的溶解度随温度变化不同 | |
| C. | 不饱和溶液转化为饱和溶液,其溶质质量分数一定变大 | |
| D. | 向氯化铁溶液中加入少量生石灰,原溶液中溶质的溶解度和溶质质量分数都发生变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
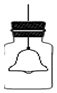 把一个小铃通过细线固定在盛满SO2的集气瓶中,向瓶中倒入NaOH溶液,迅速塞紧并轻轻振荡,过一会儿,再摇动集气瓶,只看到小铃的振动,却听不到铃声.试运用所学的科学知识进行解释.
把一个小铃通过细线固定在盛满SO2的集气瓶中,向瓶中倒入NaOH溶液,迅速塞紧并轻轻振荡,过一会儿,再摇动集气瓶,只看到小铃的振动,却听不到铃声.试运用所学的科学知识进行解释.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 敞口放置的氢氧化钠溶液易吸收空气中的二氧化碳而变质,请写出此过程的化学方程式:,现向一定质量且部分变质的氢氧化钠溶液中逐滴加入稀盐酸,并震荡.如图表示反应过程中溶液质量随加入盐酸质量的变化而变化的情况.那么,图线BC段对应的实验现象是有气泡生成,在C点时溶液中的溶质是NaCl.
敞口放置的氢氧化钠溶液易吸收空气中的二氧化碳而变质,请写出此过程的化学方程式:,现向一定质量且部分变质的氢氧化钠溶液中逐滴加入稀盐酸,并震荡.如图表示反应过程中溶液质量随加入盐酸质量的变化而变化的情况.那么,图线BC段对应的实验现象是有气泡生成,在C点时溶液中的溶质是NaCl.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com