
【题目】(8分)有一包粉末,已知由CaCO3、FeCl3、MgCl2、Na2SO4、NaOH、NaNO3中的几种组成。为确定其组成,现进行以下实验,各步骤均已充分反应。

①取一定质量的粉末,加水搅拌后过滤,得到沉淀和无色溶液A;
②向①步得到的沉淀中加入足量稀盐酸,得到无色气体和黄色溶液;
③将①步得到的无色溶液A进行如下图所示的实验。
请回答下列问题:
(1)B的化学式是 。
(2)A中一定存在的溶质的化学式是 。
(3)生成白色沉淀D的化学方程式是 。
(4)这包粉末中可能含有物质的化学式是 。
【答案】(1)BaSO4 (2)MgCl2、Na2SO4 (3)MgCl2+2AgNO3==2AgCl↓+Mg(NO3)2 (4)NaNO3
【解析】
试题分析:①取一定质量的粉末,加水搅拌后过滤,得到沉淀和无色溶液A;具体无法确定是否含有哪种物质;②向①步得到的沉淀中加入足量稀盐酸,得到无色气体和黄色溶液,证明一定含有碳酸钙、氯化铁和氢氧化钠;由③的操作可知,物质中含有硫酸钠和氯化镁;故(1)B的化学式是BaSO4 (2)A中一定存在的溶质的化学式是MgCl2、Na2SO4 (3)生成白色沉淀D的化学方程式是MgCl2+2AgNO3==2AgCl↓+Mg(NO3)2(4)这包粉末中可能含有物质的化学式是NaNO3


 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:初中化学 来源: 题型:
【题目】甲、乙两种固体纯净物的溶解度曲线如图A所示。在常温下,先在两支试管里分别装入甲、乙两种物质的饱和溶液(试管底部均有未溶解的固体),再放进盛有冰水的烧杯里(图B).下列说法正确的是( )
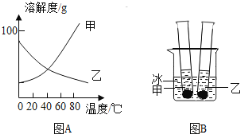
A.乙溶液中溶质的质量分数增大
B.装甲溶液的试管中剩余的固体减少
C.试管里甲、乙物质的溶解度都增大
D.两支试管里剩余的固体都增多
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是对生成氯化钠反应关系的归纳与整理。
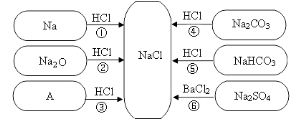
(1)物质A 是常见的碱,写出A 的化学式: 。
(2)反应④的类型为: _______ ___ 。
(3)说出NaHCO3在医疗上的一种用途:___________________________ 。
(4)反应③、④、⑤、⑥能够进行的原因是___________________________ 。
(5)实验室配制200g 8 %的NaCl 溶液,需要水的质量是________g ,配制过程中为了加快NaCl 的溶解,可以采取的措施是___________________________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C三种固体物质在水中的溶解度曲线如右图所示,请回答:

(1) ℃时,A、B两种物质在100g水中达到饱和状态时溶解的质量相等;
(2)若B中混有少量的A,最好采用 的方法提纯B;
(3)现有接近饱和的C物质溶液,使其变成饱和溶液的方法有:①加入C物质;②恒温蒸发溶剂;③ ;
(4)t3℃时将20g A物质放入50g水中,充分搅拌,所得溶液中溶质的质量分数是 ;
(5)将t3℃时等质量的A、B、C三种物质的饱和溶液降温至t1℃时,所得溶液的质量由大到小的顺序是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】取锌、铜的混合物8g与154.7g稀硫酸恰好完全反应,称得剩余物质的总质量为162.5g。
请计算:
(1)产生氢气的质量是多少?
(2)反应后所得溶液中溶质的质量分数是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】进行量筒里液体读数时,开始仰视读数为29.0mL,倒出一部分液体后,平视读数为12.7mL,则实际倒出的液体体积为
A.16.3mL B.大于16.3mL C.小于16.3mL D.无法确定
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高速铁路可以加快出行步伐。2015年12月6日,南京至安庆高铁将正式开通运营,使苏、皖、赣、鄂四省连为一体。结合所学化学知识,回答下列问题:
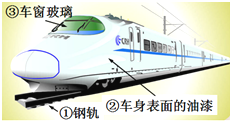
(1)图中标示的物质中为金属材料的是
(填序号),动车电路中的导线大多是用铜制的,这是利用了铜的延展性和 性。
(2)动车表面喷漆主要是为了防止外壳生锈,其原理是 。
(3)修建铁路所需的大量钢铁是以铁矿石为主要原料冶炼而得。写出一氧化碳和赤铁矿炼铁的化学反应方程式 。
(4)高铁列车车厢是密闭的空间,因此提供清洁的空气、保持车厢卫生非常重要。高铁酸钠(Na2FeO4)是高铁列车上常用的一种“绿色环保高效”消毒剂,其中高铁酸钠中铁元素化合价为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2016年3月22日是第二十届届“世界水日”,主题是“水与就业”。
(1)根据下图回答问题。
![]()

①A图所示的是水的电解实验,试管2中收集的气体是 (填名称)。
②B图所示的是活性炭净水器的示意图,其中活性炭的作用是 、
③C、D图所示的是探究铁生锈条件的实验,一段时间后发现C中铁片变红,D中铁片依然光亮,对比C、D中的现象,说明决定铁生锈快慢的一个重要因素是: 。
④E图所示的是探究燃烧条件实验,其中热水作用 、 。
(2)若用质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3)配制110g质量分数为
5%的氢氧化钠溶液。
①计算:需10%的氢氧化钠溶液体积为 mL。
②量取:用量筒量取氢氧化钠溶液和水,均倒入烧杯中。若量取氢氧化钠溶液读数时俯视,而其余操作均正确,这样配得的溶液的溶质质量分数会 (填“偏高”、“偏低”或“无影响”);用量筒量取水。
③混匀:用玻璃棒搅拌,使氢氧化钠溶液和水混合均匀。
④装瓶并贴上标签。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com