
| 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | |
| 稀盐酸质量/克 | 20 | 40 | 60 |
| 生成气体质量/克 | 2.2 | m | 5.5 |
分析 (1)根据实验数据分析可知20克稀盐酸完全反应生成二氧化碳的质量为2.2g,所以40g盐酸完全反应生成二氧化碳质量为4.4g;
(2)根据图表中数据可知最多生成二氧化碳质量为4.4g,根据二氧化碳的质量可算出碳酸钠的质量,进一步可求出混合液中碳酸钠的质量分数.
解答 解:
(1)20克稀盐酸完全反应生成二氧化碳的质量为2.2g,所以40g盐酸完全反应生成二氧化碳质量为4.4g;故填:4.4;
(2)根据前两组实验数据分析可知每20克盐酸完全反应生成2.2克二氧化碳,则60克盐酸完全反应应生成6.6克二氧化碳,在第三组实验中加入60克盐酸只生成5.5克二氧化碳,说明第三组实验中盐酸有剩余,碳酸钠反应完,完全反应生成气体的质量为5.5克,设生成5.5g二氧化碳,需要参加反应的碳酸钠的质量为x,则:
Na2CO3 +2HCl=2NaCl+CO2↑+H2O
106 44
x 5.5g
根据:$\frac{106}{x}=\frac{44}{5.5g}$
解得y=13.25g,
混合液中碳酸钠的质量分数是:$\frac{13.25g}{50g}$×100%=26.5%;
答:混合液中碳酸钠的质量分数是26.5%.
点评 解答本题可用数据分析法,即解题时正确分析数据,找出数据的变化特征及彼此之间的关系,将综合复杂的问题分解为简单的计算,从而顺利解题.


科目:初中化学 来源: 题型:实验探究题
 硫酸镁溶液可以和氢氧化钠溶液反应
硫酸镁溶液可以和氢氧化钠溶液反应 SO42-
SO42-  Mg2+
Mg2+  Na+
Na+查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 我们在探究物质燃烧的条件时,向在盛有80℃热水的烧杯底部的白磷通入氧气时,奇迹发生了:白磷在水下燃烧起来,写出该化学反应方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.待温度恢复至室温时,向水中滴加紫色石蕊试液,你预测会显红色,写出发生该现象的化学反应方程式P2O5+3H2O=2H3PO4.
我们在探究物质燃烧的条件时,向在盛有80℃热水的烧杯底部的白磷通入氧气时,奇迹发生了:白磷在水下燃烧起来,写出该化学反应方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.待温度恢复至室温时,向水中滴加紫色石蕊试液,你预测会显红色,写出发生该现象的化学反应方程式P2O5+3H2O=2H3PO4.查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 反应物的温度、浓度、固体反应物的颗粒大小等因素会影响化学反应速率.为研究实验室制取二氧化碳的适宜条件,进行如下四组实验:
反应物的温度、浓度、固体反应物的颗粒大小等因素会影响化学反应速率.为研究实验室制取二氧化碳的适宜条件,进行如下四组实验:| 甲 | 乙 | 丙 | 丁 | |
| 大理石/(等量) | 块状 | 块状 | 粉末状 | 粉末状 |
| 盐酸/(质量分数) | 5% | 10% | 5% | 10% |
| 收集50mL二氧化碳所需时间/(秒) | 118 | 60 | 70 | 50 |
| 时段 | 第10秒 | 第20秒 | 第30秒 | 第40秒 | 第50秒 | 第60秒 |
| CO2体积 | 13 | 11 | 9 | 8 | 5 | 4 |
| 甲 | 乙 | |
| 大理石/(等量) | 块状 | 块状 |
| 盐酸/(质量分数) | 10% | 10% |
| 盐酸质量/(g) | 100 | 100 |
| 盐酸温度/℃ | 20 | 30 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验记录 | 实验结论 |
| ①取少量黑色粉末于试管中,滴加少量无色溶液 ②用带火星的木条放在试管口 | ①气泡产生 ②木条复燃 | 产生的气体是氧气, 原猜想①成立. |
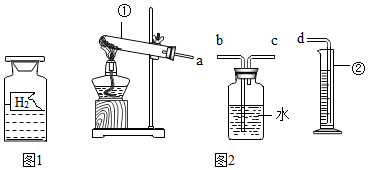
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com