
用16 g溶质质量分数为25%的氢氧化钠溶液,恰好完全中和20 g的硫酸溶液.求:
(1)此硫酸溶液中溶质的质量分数;
(2)反应后溶液中溶质的质量分数.
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| 密度(ρ)/g?ml-1 | 1.00 | 1.02 | 1.04 | 1.06 | 1.08 | 1.10 | 1.12 | 1.14 | 1.16 | 1.185 |
| 溶质质量分数(w)/% | 0.4 | 4.4 | 8.5 | 12.5 | 16.5 | 20.4 | 24.2 | 28.2 | 32.2 | 37.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:
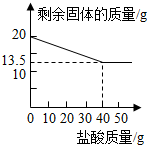 如今市场上出现的假黄金(铜锌合金)坑害了许多消费者.某校化学兴趣小组的同学们为测定假黄金的组成,称取20克假黄金置于烧杯中,用某未知溶质质量分数的稀盐酸50克,分5次加入,每次充分反应后,取出固体,经过滤、干燥等操作后称重,各次稀盐酸用量和剩余固体质量记录如下:
如今市场上出现的假黄金(铜锌合金)坑害了许多消费者.某校化学兴趣小组的同学们为测定假黄金的组成,称取20克假黄金置于烧杯中,用某未知溶质质量分数的稀盐酸50克,分5次加入,每次充分反应后,取出固体,经过滤、干燥等操作后称重,各次稀盐酸用量和剩余固体质量记录如下:| 实验次数 | 稀盐酸的用量(g) | 剩余固体的质量(g) |
| 1 | 10 | 18.375 |
| 2 | 10 | 16.750 |
| 3 | 10 | 15.125 |
| 4 | 10 | 13.500 |
| 5 | 10 | 13.500 |
查看答案和解析>>
科目:初中化学 来源: 题型:
(8分)以下是某研究小组探究影响反应速率部分因素的相关实验数据。
| 实验序号 | H2O2溶液溶质质量分数% | H2O2溶液体积/mL | 温度℃ | MnO2的用量/g | 收集氧气的体积/mL | 反应所需 的时间/s[ |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 4.04 |
| ③ | 30 | 5 | 20 | 0.1 | 2 | 49.21 |
| ④ | 30 | 5 | 20 | 0.5 | 2 | 10.76 |
(1)通过实验①和②对比可知,化学反应速率与 有关;
从实验 和 对比可知,化学反应速率与催化剂的关系是:
。
(2)化学反应的实质是微观粒子相互接触、碰撞的结果,化学反应速率与微观粒子的概率有关。试从微观角度解释“反应物浓度越大,化学反应速率越快”的原因是:
。(2分)
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总重量 (选填“减小”或“不变”或“增大”)。
(4)还有哪些因素可能影响该反应的速度呢?
请说出你的一个猜想: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
(4分)下图为a、b两种物质在水中的溶解度曲线。

(1)10℃时,a的溶解度_________b的溶解度(填 “>”、“<”或“=”) 。
(2)30℃时,两种物质的溶解度曲线有交点,由此可获取的信息是:________________。
(3)若要将溶液中的溶质分离出来,可以采用蒸发结晶和降温结晶等方法。上述两种物质中,较适合用降温结晶的是_______(填“a”或“b”)。
(4)要把100g溶质质量分数为20%的b物质的溶液稀释为溶质质量分数为16%的b物质的溶液,需要加入水_______g。
查看答案和解析>>
科目:初中化学 来源: 题型:
(7分)实验室需配制4%的氢氧化钠溶液200g,并用此溶液测定某敞口放置一段时间的盐酸的溶质质量分数。
(1)配制200g质量分数为4%的氢氧化钠溶液,需要氢氧化钠固体的质量为 ▲ g,水的体积为 ▲ mL(水的密度近似看作1g/cm3)。
 (2)取10g此盐酸于烧杯中,逐滴滴加溶质质量分数为
(2)取10g此盐酸于烧杯中,逐滴滴加溶质质量分数为
4%的氢氧化钠溶液,用pH计(一种测定溶液pH的仪器)
测定溶液的pH,得到的数据如下:
| 加入氢氧化钠 的体积/mL | 0 | 1.0 | 8.0 | 9.5 | 10.5 | 12.0 | 16.5 |
| 烧杯中溶液pH | 1.0 | 1.3 | 2.0 | 3.9 | 9.9 | 11.9 | 12.8 |
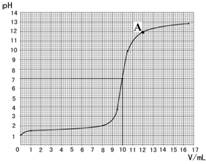
依据表中数据绘制出烧杯中溶液的pH与加入氢氧
化钠溶液体积(V)之间的变化关系图。
(3)根据上图查出氢氧化钠与盐酸恰好完全反应时,所滴加氢氧化钠溶液的体积为 ▲ mL,A点所表示的溶液中溶质的化学式为 ▲ 。
(4)计算此瓶盐酸的溶质质量分数。(请写出计算过程。氢氧化钠溶液的密度按1.0g/mL计算)
▲
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com