

 Cu+H2O,D中的水其实是C中反应产生的水,装置C的玻璃管和其中固体的总质量在反应后减少了1.6g,其实质是CuO中氧元素的质量为1.6g;装置D的干燥管和其中物质的总质量在反应后增加了1.82g,其实质是产生水的总质量为1.82g,故氢元素质量为1.82-1.6=0.22g,所以水中H、O元素的质量比=0.22:1.6=11:80 ;
Cu+H2O,D中的水其实是C中反应产生的水,装置C的玻璃管和其中固体的总质量在反应后减少了1.6g,其实质是CuO中氧元素的质量为1.6g;装置D的干燥管和其中物质的总质量在反应后增加了1.82g,其实质是产生水的总质量为1.82g,故氢元素质量为1.82-1.6=0.22g,所以水中H、O元素的质量比=0.22:1.6=11:80 ;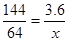 x=" 1." 6g
x=" 1." 6g

 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:初中化学 来源:不详 题型:填空题
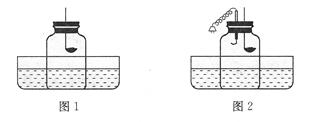
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
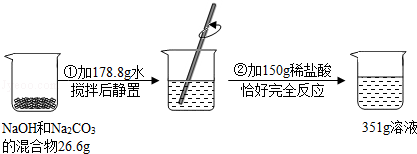
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
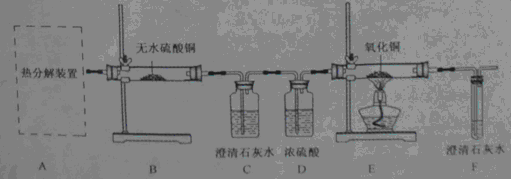

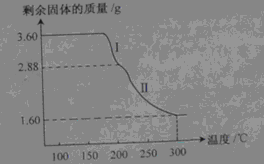
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
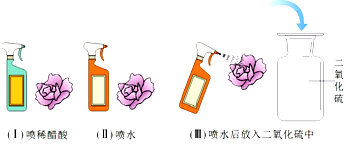
| 实验操作 | 实验现象 |
| | |
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验步骤 | 实验操作 | 实验现象 | 实验结论 |
| (1) | 向装有氢氧化钠溶液的试管中滴加酚酞溶液 | 溶液变为红色 | |
| (2) | | | |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
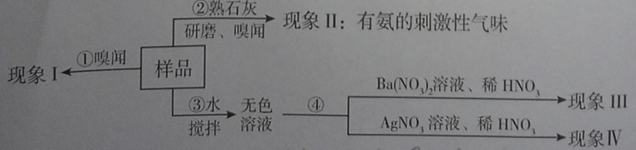
| | 假设和现象 | 判断和化学方程式 |
| a | 若现象I为无氨味。 | 则样品中不含________________(填名称)。 |
| b | 由操作②现象判断。 | 该样品一定含有__________离子。 |
| c | 若现象Ⅲ为白色沉淀,现象Ⅳ为无沉淀。 | 则样品中含有 (写名称),该反应的化学方程式为 。 |
| d | 若现象Ⅲ为“无沉淀”,现象Ⅳ为白色沉淀。 | 则样品中含有 (写化学式),该反应的化学方程式为 。 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com