
【题目】图中A、B、C、D是四种拉子的结构示意图,E为氬元素在元素周期表中的信息示意图。
(1)B元素属于(填“金属”或“非金属”)_____元素;A元素的质子数为_____。
(2)图中A、B、C、D四种粒子表示原子的是_____,表示阳离子的是_____。
(3)图中A、B、C、D四种粒子表示稳定结构的是为_____。
(4)对E中提供的信息理解正确的是_____。
①属于金属元素②中子数为18③核电荷数为18④相对原子质量为40
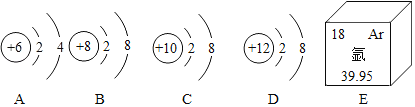
科目:初中化学 来源: 题型:
【题目】在化学王国里,数字被赋予了丰富的内涵。对下列化学用语中数字“2”的说法正确的( )
①2H ②2NH3 ③SO2 ④![]() ⑤2OH-⑥H2O
⑤2OH-⑥H2O
A. 表示分子个数的是①②
B. 表示分子中原子个数的是③⑥
C. 表示离子的个数的是④⑤
D. 表示离子所带电荷数的是④⑥
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】![]() 是初中常见的8种物质,它们有如图所示的转化关系、已知A、C是无色液体,B、F、G是无色气体,其中大量排放F会引起温室效应,D是黑色固体,E在纯净的B中燃烧发出明亮的蓝紫色火焰。
是初中常见的8种物质,它们有如图所示的转化关系、已知A、C是无色液体,B、F、G是无色气体,其中大量排放F会引起温室效应,D是黑色固体,E在纯净的B中燃烧发出明亮的蓝紫色火焰。
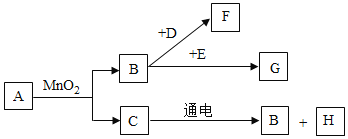
![]() 请写出下列物质的化学式:D______,E______,G______,H______。
请写出下列物质的化学式:D______,E______,G______,H______。
![]() 请写出下列变化的化学方程式:
请写出下列变化的化学方程式:![]() ______。
______。
![]() 物质F在生活中的用途:______。
物质F在生活中的用途:______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常见制取氧气的方法有:
(一)加热氯酸钾 (二)加热高锰酸钾 (三)分解过氧化氢。
其实验装置如图所示。
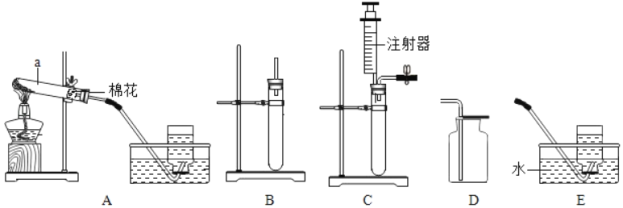
(1)装置A中仪器a的名称是:_____;
(2)如图装置A正在制取氧气,则制取氧气的方法是上述三种方法中的①_____,发生反应的化学方程式为②_____,收集氧气时集气瓶内要装满水的目的是③_____;
(3)实验室用加热的方法制取氧气的过程,大致可分以下几步,其中正确顺序是_____;
①点燃酒精灯给试管加热 ②熄灭酒精灯 ③检验装置的气密性 ④将药品装入试管并固定装置 ⑤用排水法收集气体 ⑥将导气管从水槽中移出
A.③④①⑤②⑥ B.③④①⑤⑥② C.④①③⑤②⑥ D.④①③⑤⑥②
(4)用装置D收集一瓶氧气,验满的操作是_____;
(5)从环保、节能、操作简单的角度分析,制取氧气时最好选用上述三种方法中的_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】溶液与人们的生活息息相关。
(1)下列少量物质分别放入水中,充分搅拌,可以得到溶液的是______(填字母)。
A.高锰酸钾 B.汽油 C.面粉
(2)下表是三种物质在不同温度时的溶解度,根据表中信息回答问题。
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | 氯化钠 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
硝酸钾 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
氢氧化钙 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 | |
①60℃时,氯化钠的溶解度_______硝酸钾的济解度(填“>”“=”或“<”)。
②向20℃的氢氧化钙饱和溶液中加入少量生石灰,再冷却至20℃,此时溶液中溶质的质量比加入生石灰前溶液中溶质的质量____(填“增大”“不变”或“减小”)。
③混有少量氯化钠的硝酸钾固体,加水配成80℃的硝酸钾饱和溶液,再冷却至20℃,析出晶体并得到溶液。下列有关说法中正确的是_______(填字母)。
A.析出的晶体中不一定含有硝酸钾
B.所得溶液一定是硝酸钾饱和溶液
C.上述方法可以将两种物质完全分离
(3)如图所示为X、Y、Z三种固体物质(不含结晶水)的溶解度曲线,请回答下列问题:
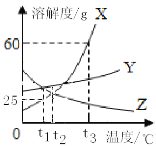
①t3℃时,溶质质量分数为25%的X溶液降温到t1℃,所得溶液中溶质质量分数是________。
②t3℃时,等质量X、Y、Z的饱和溶液分别降温到t1℃,溶液质量没有变化的是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】蛋白质在人体胃肠内与水反应,最终生成氨基酸被人体吸收。丙氨酸(化学式为C3H7O2N)就是其中的一种。请回答下列问题:
(1)丙氨酸分子中,碳、氢、氧、氮四种原子的个数比是_____。
(2)丙氨酸的相对分子质量是_____。
(3)氮元素质量分数是_____。
(4)89g谷氨酸中的氮元素与_____g尿素[CO(NH2)2]中所含的氮元素相等。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸钠在轻工、建材、纺织、国防、医药等工业中有重要的应用,我国化学家侯德榜创立了著名的“侯氏制碱法”,促进了世界技术的发展。
(查阅资料)①生产原料粗盐中含有少量可溶性杂质(MgCl2 和 CaC12)及不溶性杂质。
②氨气极易溶于水,二氧化碳能溶于水。
③生产原理:NaCl + NH3 + CO2+ H2O = NaHCO3↓+ NH4C1,分离得晶体 A,并使其充分受热,可分解制得纯碱及两种常见的氧化物。
④氯化铵分解的化学方程式是 NH4Cl===NH3↑+HCl↑。
⑤部分生产流程如下图所示:
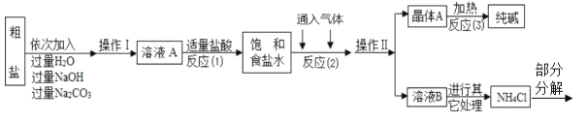
(问 题讨论)
(1)溶液 A 中的溶质为 ________,流程中加入适量盐酸的作用是 ________。
(2)反应(2)中为提高产率,所通入气体的顺序是 ________(填字母序号).
A.先通入 CO2 再通入 NH3 B.先通入 NH3 再通入 CO2
(3)上述生产流程中可循环使用的是 ________(填序号).
A.CO2 B.NH3 C.HCl D.NaOH E.Na2CO3
(组成确定)
(1)称取一定质量的纯碱样品,多次充分加热,称重,质量无变化;
(2)另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀 HNO3,再滴加 AgNO3溶液,有白色沉淀。由上述实验可确定纯碱样品含有杂质 ________(写化学式).
(含量测定) 同学们为了测定该纯碱样品的纯度(假定只含一种上述杂质),设计了如下三组实验。甲组:取 12.0g 纯碱样品,向其中加入过量的盐酸,直至样品中无气泡冒出。将反应所得溶液小心蒸发,并将所得物质干燥、冷却至室温称得固体质量为 13.1g.样品中碳酸钠的质量分数为________。
乙组:取 12.0g 纯碱样品,利用下图所示装置,测出反应装置 C 增重了 4.1g(所加试剂均足量,每一步都反应完全).实验结束,发现乙组测定的质量分数偏小,其原因是_________。
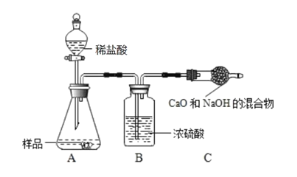
丙组:取 12.0g 的纯碱样品,完全溶于水,向其中加入过量的氯化钙溶液,待完全沉淀过滤、 洗涤、烘干称量固体质量,从而计算出碳酸钠的质量分数。组内同学提出意见,认为如果将氯化钙溶液换成氯化钡溶液则更好,老师认为有道理,原因是 ________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列粒子结构示意图,回答问题。
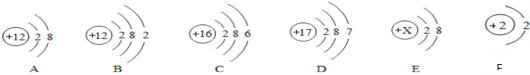
(1)上图A、B、C、D四种粒子共表示_____种元素;
(2)D原子在化学反应中易_____(填“得到”或“失去”)电子;
(3)上图从A至F中达到相对稳定结构的是_____;
(4)E粒子带1个单位负电荷,则X=_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com