
 小丽同学取铜和氧化铜的混合物mg置于烧杯中,并向烧杯中逐滴加入稀硫酸溶液,不断搅拌,测得烧杯中溶液的质量与加入稀硫酸的质量关系如图所示.求:
小丽同学取铜和氧化铜的混合物mg置于烧杯中,并向烧杯中逐滴加入稀硫酸溶液,不断搅拌,测得烧杯中溶液的质量与加入稀硫酸的质量关系如图所示.求:| 溶质质量 |
| 溶液质量 |
| 80 |
| 8g |
| 160 |
| x |
| 16g |
| 57g |


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案科目:初中化学 来源: 题型:
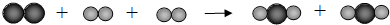
| A、化学反应前后原子种类、数目不变 |
| B、化学反应前后元素的种类、质量未发生变化 |
| C、该反应中,分子的个数比为1:2:2 |
| D、该反应不属于基本类型反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com