
分析 根据消耗的稀盐酸的质量结合反应的化学方程式可以计算出碳酸钙的质量和生成氯化钙的质量,进而求算出样品中碳酸钙的质量分数和反应后所得溶液中溶质的质量分数;
解答 解:设6g样品中CaCO3的质量为x,生成氯化钙的质量为y,
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 73 111 44
x 36.5g×10% y z
$\frac{100}{x}=\frac{73}{36.5g×10%}=\frac{111}{y}$ $\frac{44}{z}=\frac{73}{36.5g×10%}$
x=5g
y=5.55g
z=0.22g
(1)样品中碳酸钙的质量分数:$\frac{5g}{6g}×100%$=83.3%;
(2)反应后所得溶液中溶质的质量分数:$\frac{5.55g}{5g+36.5g-0.22g}×100%$=13.4%;
答:(1)样品中碳酸钙的质量分数83.3%;
(2)反应后所得溶液中溶质的质量分数13.4%.
点评 要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.


科目:初中化学 来源: 题型:填空题
 ”表示氨原子,“
”表示氨原子,“ ”表示氢原子),请在“反应后”框内将相关粒子的图形补充完整.
”表示氢原子),请在“反应后”框内将相关粒子的图形补充完整.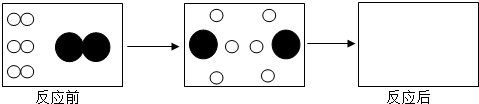
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe、Cu、Ni | B. | Ni、Fe、Cu | C. | Fe、Ni、Cu | D. | Cu、Ni、Fe |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 .请回答下列问题:
.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com