
分析 (1)相对分子质量等于各个原子相对原子质量的总和;
(2)根据学过的知识要知道它们的密度大小,不需要记住它们的具体数值,能比较出它们的大小即可;
(3)根据空气中各成分的体积分数解答.
解答 解:相对分子质量分别为:①二氧化碳:12+16×2=44,②氢气:1×2=2,③氮气:14×2=28,所以相对分子质量从大到小:①③②;
(2)根据学过的知识经验可知,密度最小的就是氢气,氧气的密度又比空气的密度大,所以从大到小的顺序是:①③②;
(3)空气的成分及各成分的体积分数分别是:“氮气78%、氧气21%、稀有气体0.94%、二氧化碳0.03%、其他气体和杂质0.03%,则由多到少的顺序是:②①③④;
故答案为:(1)①③②;(2)①③②;(3)②①③④.
点评 掌握相对分子质量的计算方法,及常见气体的密度、空气的成分及体积分数,即可结合题意正确解答.


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
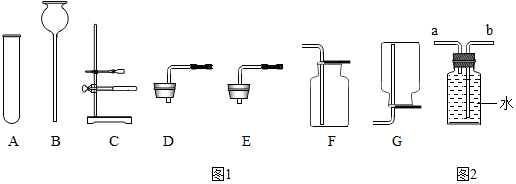
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
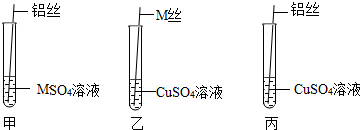
| 实验操作 | M丝插入试管①中 | 铜丝插入试管②中 | 铝丝插入试管③中 | 实验结论 |
| 刚开始的现象 | 有少量气泡产生 | 无气泡 | 无气泡 | M>Cu:M>Al |
| 几分钟后的现象 | 有少量气泡产生 | 无气泡 | 有大量气泡产生 | Al>M>Cu |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验序号 | 实验方法与操作 | 实验现象 | 结论 |
| ③ | 将少许Cu(OH)2粉末加到5mL蒸馏水中,充分振荡 | 沉淀不溶解 | 猜想一错误 |
| ④ | 将少许Cu(OH)2粉末加到NaOH浓溶液中,充分振荡 | 沉淀溶解 | 猜想二正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | CH3COOH | B. | H2O和CO2 | C. | O2和H2O | D. | C2H2 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
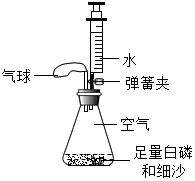 实验小组利用如图所示装置测量空气中氧气体积分数并取得成功.
实验小组利用如图所示装置测量空气中氧气体积分数并取得成功.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图是化肥硝酸铵包装袋上的部分说明:
如图是化肥硝酸铵包装袋上的部分说明:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 0.5 X% | B. | 1-0.5 X% | C. | 2 X% | D. | 1-7 X% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com