
(6 分)镁是一种用途广泛的金属材料,目前大部分镁都是利用从海水中提取的镁盐 制取的。某校化学活动小组欲测定海水中氯化镁的含量,取海水样品 200g,加入适量 氢氧化钠溶液,至恰好完全反应为止,称量所得沉淀物的质量为 0.58g。 请你根据上述资料,回答下列问题:
⑴金属镁的物理性质有: 。(答出一条即可)
⑵查阅资料可知,海水中镁元素的含量比较低,所以,从海水中提取 MgCl2 时, 经历了“MgCl2 → Mg(OH)2 → MgCl2”的转化过程,请分析这样做的目的是
⑶列式计算:上述 200g 海水样品中,所含 MgCl2 的质量是多少?
(提示:MgCl2 + 2NaOH = Mg(OH)2↓ + 2NaCl )
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:初中化学 来源: 题型:单选题
将一块质量为10 g的铜锌合金投入到盛有100g稀硫酸的小烧杯中,恰好完全反应,称的小烧杯中剩余物的总质量为109.8克。请你据此分析并列式计算:
(1)生成氢气的质量为 克。
(2)该铜锌合金中铜的质量为多少克?
(3)求所用稀硫酸中溶质的质量分数?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
向50g Na2CO3溶液中逐滴加入一定溶质质量分数的CaCl2溶液。实验过程中,生成沉淀质量与加入CaCl2溶液的质量关系如右图所示,试计算:
(1)恰好完全反应时,生成沉淀的质量为______________g。
(2)计算恰好完全反应时,所得溶液中溶质的质量分数。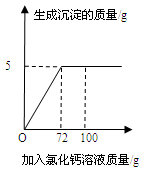
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
请回答下列与金属有关的问题:
(1)生铁片与纯铁片相互刻画时,纯铁片表面可留下划痕,说明 的硬度大;
(2)6.5g与足量的稀硫酸反应(化学方程式为Zn+H2SO4═ZnSO4+H2↑),理论上可制得氢气的质量
为 g.
(3)使用下列各组试剂,能验证Fe、Cu、Ag活动性顺序的是
A.Ag、FeSO4溶液、CuSO4溶液
B.Fe、Cu、AgNO3溶液
C.Fe、Ag、CuSO4溶液.
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(7分)兴趣小组的同学为测定某一铁铜合金中含铁的质量分数,将6g该合金粉末样品,加入溶质质量分数为10%的硫酸铜溶液160g中,二者恰好完全反应。同时为了充分利用资源,还对反应后的物质进行回收处理。请结合下列图示计算:
(1)该合金样品中含铁的质量分数;(计算结果精确至0.1%)
(2)所的固体铜的质量a为多少g?
(3)向不饱和滤液中加入多少g水,能得到5%的硫酸亚铁溶液,用于花卉的营养液。
((2)(3)中计算结果精确至0.1g)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(7分) 某学生做了如下图所示的实验。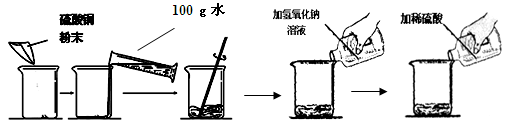
| | 第一次 | 第二次 |
| 加入硫酸铜的质量 | m | m |
| 加入氢氧化钠溶液的质量 | 50g(溶质质量分数16%) | 50g(溶质质量分数16%) |
| 加入稀硫酸的质量 | 50g | 100g |
| 实验现象 | 蓝色固体和蓝色溶液 | 蓝色溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(7分)水是生命之源,爱护、珍惜水资源是每个公民的责任。
(1)自然界中的水不是纯水,可利用沉淀、 、吸附和蒸馏等方法可以净化水。
(2)水常用来配制各种溶液,下列物质溶于水后溶液温度明显升高的是 。
| A.氢氧化钠 | B.硝酸钾 | C.硝酸铵 | D.浓硫酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
((7分)某纯碱样品中混有少量的氯化钠,为了测定该样品中碳酸钠的质量分数,小明同学准确称取 12.0g样品,做了如下实验: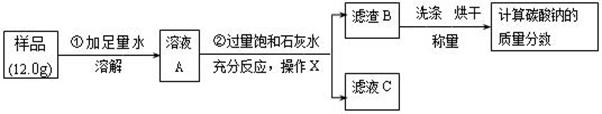
请回答下列问题:
(1)操作X用到的玻璃仪器除烧杯、玻璃棒外,还必需有 。
(2)滤液 C中的溶质是 ,若向滤液 C中滴加稀盐酸,写出过程中发生的一个中和反应的化学方程式 。
(3)若将滤渣B洗涤烘干后,称量其质量为 10.0g , 计算纯碱样品中的 Na2CO3的质量分数是多少?(结果保留一位小数,要求写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(3分)实验室有一瓶硫酸废液,老师请小红同学设计方案测定该废液中硫酸的质量分数。小红同学先取一洁净小烧杯,称其质量为18.2g,然后往其中倒入适量的硫酸废液后称量,总质量为33.2g,之后,将一枚质量为10.8g的铁钉(已用砂纸打磨去掉铁锈)放入该小烧杯中反应,当反应后的溶液呈中性时再次称量,总质量为43.9 g。请回答下列问题:
反应中产生的气体的质量是。
计算该废液中硫酸的质量分数(写出计算过程,计算结果保留一位小数)。
如果铁钉的铁锈未除净,对计算结果的影响是 (选填“偏大”、“偏小”、“无影响”) 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com