
【题目】化学是一门以实验为基础的学科,化学所取得的丰硕成果,与实验的重要作用分不开。结合下列实验装置图回答问题:
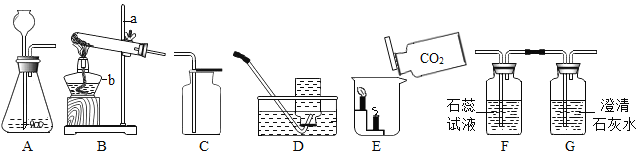
(1)写出图中有标号的仪器名称:a__________________、b______________。
(2)写出实验室用B装置制取氧气发生的化学反应方程式________________________________。
(3)若装置A中反应剧烈,从实验安全角度考虑,可以将长颈漏斗换成________________来控制液体的滴加速度。
(4)欢欢同学制取了一瓶二氧化碳气体,按图E进行实验,观察到的现象是_______________________,实验说明二氧化碳的性质有__________________________________________________________________。(至少写出两条)。
(5)梅梅同学用图中A、F、G装置组合制取二氧化碳气体并验证相关性质。
①写出制取二氧化碳气体反应方程式__________________________________________________________,
②F装置中反应现象是_______________________________________________________________________,
③G装置中发生的化学反应方程式为__________________________________________________________。
【答案】铁架台 酒精灯 2KClO3![]() 2KCl+3O2↑ 分液漏斗 蜡烛由低到高逐渐熄灭 不可燃、不助燃,密度比空气的大 CaCO3+2HCl=CaCl2+H2O+CO2↑ 溶液由无色变成红色 CO2+Ca(OH)2=CaCO3↓+H2O
2KCl+3O2↑ 分液漏斗 蜡烛由低到高逐渐熄灭 不可燃、不助燃,密度比空气的大 CaCO3+2HCl=CaCl2+H2O+CO2↑ 溶液由无色变成红色 CO2+Ca(OH)2=CaCO3↓+H2O
【解析】
(1)由所学知识可知,图中有标号的仪器名称:a铁架台、b酒精灯;
(2)实验室用加热氯酸钾制取氧气时常用B装置,氯酸钾在二氧化锰的作用下分解生成氯化钾和氧气,化学反应方程式2KClO3![]() 2KCl+3O2↑;
2KCl+3O2↑;
(3)若装置A中反应剧烈,从实验安全角度考虑,可以将长颈漏斗换成分液漏斗,通过控制活塞开启的程度来控制液体的滴加速度,进而控制反应速率,使反应平稳;
(4)制取一瓶二氧化碳气体,按图E进行实验,观察到的现象是蜡烛由低到高逐渐熄灭,实验说明二氧化碳的性质有:不可燃、不助燃,密度比空气的大;
(5)①制取二氧化碳气体的反应原理是碳酸钙和盐酸反应生成二氧化碳、氯化钙、水,反应方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
②二氧化碳和水反应生成碳酸,酸性溶液能使紫色石蕊试液变红,F装置中反应现象是溶液变成红色;
③二氧化碳和氢氧化钙溶液反应生成碳酸钙沉淀和水,化学反应方程式为CO2+Ca(OH)2=CaCO3↓+H2O。


科目:初中化学 来源: 题型:
【题目】现有H2SO4和CuSO4的混合溶液,为了测定CuSO4的质量分数,小明同学进行如下实验:
取混合溶液于烧杯中,向其中加入铁片至完全反应。反应前后,有关数据如表。
烧杯 | 原混合溶液 | 加入的铁片 | 反应后烧和烧杯内物质的总质量(克) | 剩余铁片 | 析出铜 | |
质量(克) | 80 | 100 | 20 | 199.8 | 3.2 | 12.8 |
(1)实验中产生氢气的质量为______克。
(2)请根据实验数据计算原混合溶液中CuSO4的质量分数______。
(3)小红同学用加入足量BaCl2溶液,通过生成BaSO4沉淀的质量来计算原混合溶液中CuSO4的质量分数,请分析是否合理并说明原因______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为A、B、C、D四种粒子的结构示意图以及硒元素在元素周期表中的信息,请按要求填空:
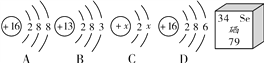
(1)A、B、C、D四种粒子中,属于同种元素的是________(填序号),C粒子的符号为________。
(2)由A元素和B元素形成的化合物的化学式为________。
(3)该硒原子的中子数是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲物质的溶液可用作化肥、电镀液等,甲的溶解度曲线如图所示,下列说法正确的是( )

A. 甲的溶解度是102.5g
B. 甲的溶解度随温度的升高而增大
C. 将70℃ 甲的饱和溶液升高温度或降低温度,都有晶体析出
D. 20℃时,100g甲的饱和溶液中溶质质量为28.6g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究.
[查阅资料]
名称 | 食用纯碱 | 食用小苏打 |
主要成分 | Na2CO3 | NaHCO3 |
酸碱性 | 水溶液显碱性 | 水溶液显碱性 |
热稳定性 | 受热不分解 | 270℃时完全分解为碳酸钠、二氧化碳、水 |
[实验探究]
(1)探究两者水溶液酸碱性的差异
小明分别向等浓度的两种溶液中滴入酚酞试液,发现两者都变_____色,但食用纯碱溶液中颜色更深,由此推测可能_____溶液碱性更强.小欢认为要比较两种溶液的碱性强弱,可直接用_____进行测定.
(2)验证两种粉末的稳定性
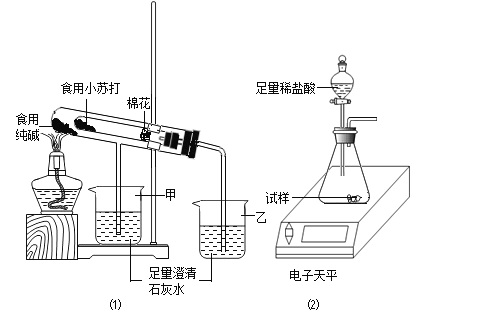
在老师的指导下,该小组按如图1装置进行实验操作,观察到_____(填“甲”或“乙”)烧杯中澄清石灰水变浑浊,试管中发生反应的化学方程式为_____,装置中棉花的作用是_____.
(3)测定食用纯碱粉末的纯度
取食用纯碱粉末试样,利用如图2装置进行实验测定.
数据记录如下:
称量项目 | 称量时间 | 质量/g |
试样 | 11.0 | |
装置+稀盐酸 | 160.0 | |
装置+稀盐酸+试样 | 反应开始后20s | 167.0 |
装置+稀盐酸+试样 | 反应开始后30s | 166.6 |
装置+稀盐酸+试样 | 反应开始后90s | 166.6 |
①反应生成CO2的质量为_____g.
②通过计算确定食用纯碱粉末中Na2CO3的质量分数____.(写出计算过程,结果保留一位小数.)
③如果测得的结果比实际纯度高,可能的原因是_____.(答一种即可)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】空气和水是一切生命赖以生存的根本,没有空气和水就没有生命。
(1)近年来大气中二氧化碳含量不断上升的主要原因是__________
(2)下列物质在水中不能形成溶液的是__________(填序号)。
①白糖 ②汽油 ③食盐 ④高锰酸钾
(3)下列水中属于纯净物的是______________。
①自来水 ②矿泉水 ③软水 ④蒸馏水
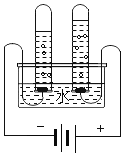
(4)下图是电解水的简易实验装置,电解水实验结论是________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)随着生活水平的提高,现在许多学校的校园内或教室里都有“直饮水”点,直饮水的主要生产流程如图所示:
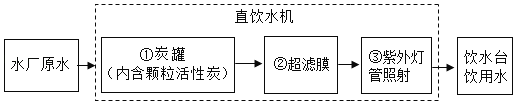
步骤①中活性炭的作用是_____;步骤②中超滤膜可以让水分子通过,其他大分子污染物则被截留,这个分离过程属于_____(填“物理变化”或“化学变化”);步骤③的目的是_____。
(2)自来水厂为了得到澄清透明、无肉眼可见物的水,通常会加入絮凝剂_____(填物质名称),用二氧化氯ClO2对自来水进行消毒杀菌,二氧化氯属于_____(填“单质”或“氧化物”)。在实验室里,常用到静置、吸附、过滤、蒸镏等操作,其中可以降低水的硬度的操作是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列曲线示意图与相应选项表示不正确的是( )
A. |
B. |
C. |
D. |
A. AB. BC. CD. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图1是甲锶元素(Sr)形成的粒子结构示意图。图2是某些粒子的结构示意图。
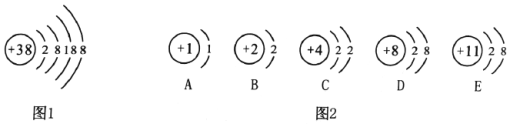
(1)图一表示的微粒符号写为_____________。
(2)由D、E两种微粒构成的物质属于________(填“酸”“碱”“盐”或“氧化物”)
(3)图2表示的某些元素可以组成一种实验室里制取氧气的物质。该物质制取氧气的化学方程式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com