
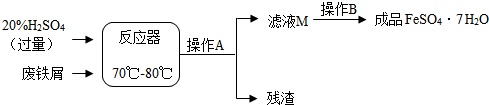
| ||
| 24 |
| x |
| 2 |
| 0.2g |
| 2.4g |
| 2.5g |
| ||


科目:初中化学 来源: 题型:
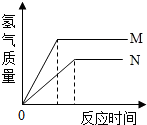 等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是( )
等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是( )| A、M、N反应消耗的盐酸质量相等 |
| B、生成H2的质量M<N |
| C、相对原子质量较大的是N |
| D、产生H2的速率N>M |
查看答案和解析>>
科目:初中化学 来源: 题型:
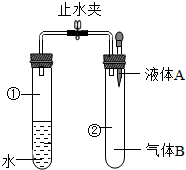 已知水的沸点随压强的减少而降低.现有如图所示实验装置,夹子开始处于关闭状态.将液体A滴入试管②与气体B充分反应后,打开夹子,发现试管①内的水立刻沸腾.A和B最不可能的一种组合是( )
已知水的沸点随压强的减少而降低.现有如图所示实验装置,夹子开始处于关闭状态.将液体A滴入试管②与气体B充分反应后,打开夹子,发现试管①内的水立刻沸腾.A和B最不可能的一种组合是( )| A、A为NaOH溶液,B为CO2气体 |
| B、A为稀H2SO4溶液,B为NH3气体 |
| C、A为AgNO3溶液,B为HCl气体 |
| D、A为CaCl2溶液,B为CO2气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:
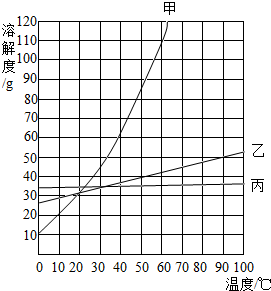 实验室需要配置一定浓度的硝酸钾溶液.
实验室需要配置一定浓度的硝酸钾溶液.| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| KNO3溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
查看答案和解析>>
科目:初中化学 来源: 题型:
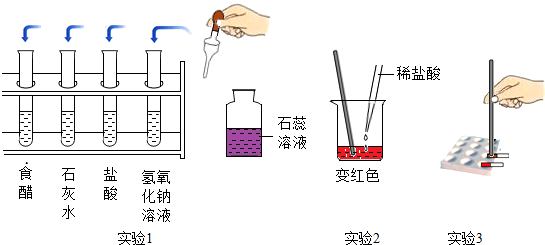
| 预计现象及相应结论 | |
查看答案和解析>>
科目:初中化学 来源: 题型:
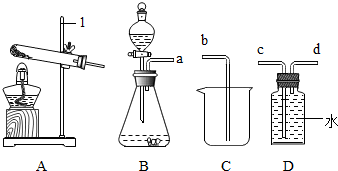 如图是实验室制取气体的装置.请根据要求回答:
如图是实验室制取气体的装置.请根据要求回答:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
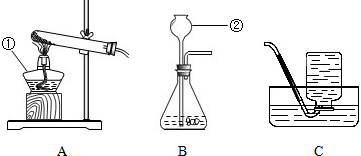
查看答案和解析>>
科目:初中化学 来源: 题型:
 化学与生活、生产密切相关.请回答下列问题:
化学与生活、生产密切相关.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com