
图是A、B、C三种物质的溶解度曲线,下列分析不正确的是( )

|
| A. | 50℃时A、B、C三种物质的溶解度由大到小的顺序是A>B>C |
|
| B. | 50℃时,把50 g A放入50 g水中能得到A的饱和溶液,其中溶质与溶液质量比为1:3 |
|
| C. | 将50℃时A、B、C三种物质的饱和溶液降温度20℃时,这三种溶液的溶质质量分数的大小关系是B>C=A |
|
| D. | 将C的饱和溶液变为不饱和溶液,可采用降温的方法 |
| 固体溶解度曲线及其作用;饱和溶液和不饱和溶液相互转变的方法.. | |
| 专题: | 溶液、浊液与溶解度. |
| 分析: | A、根据A、B、C三种固体物质的溶解度曲线比较溶解度的大小; B、根据在25℃时A物质的溶解度计算分析; C、根据A、B、C三种固体物质的溶解度随温度变化的情况及溶解度与溶液溶质质量分数的关系分析; D、根据C物质的溶解度随温度变化的情况分析将饱和溶液变为不饱和溶液,可采用的方法. |
| 解答: | 解:A、由A、B、C三种固体物质的溶解度曲线可知,在50℃时A、B、C三种物质的溶解度由大到小的顺序是A>B>C.故A正确; B、由A物质的溶解度曲线可知,在50℃时,A物质的溶解度是50g,把50g A放入50g水中能得到A的饱和溶液,能溶解25gA物质,其中溶质与溶液质量比为25g:(25g+50g)=1:3;故B正确; C、将50℃时A、B、C三种物质的饱和溶液降温度20℃时,由于A、B的溶解度随温度的降低而减小,形成的是20℃时饱和溶液,由于C的溶解度随温度的降低而增大,溶液中溶质的质量分数就是50℃时饱和溶液溶质的质量分数,由于20℃时A、B的溶解度与C物质在50℃时溶解度的大小关系是:B>A>C.所以,三种溶液的溶质质量分数的大小关系是:B>A>C.故C错误; D、由C物质的溶解度曲线可知,C物质的溶解度随温度降低而增大,所以,将C的饱和溶液变为不饱和溶液,可采用降温的方法.故D正确. 故选C. |
| 点评: | 本题考查了学生对溶解度的概念的理解以及对溶解度曲线的应用,能培养学生应用知识解决问题的能力. |


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
多彩的“碳”,多姿的生活,让我们一起走进“碳”世界:
(1)根据如表提供的信息,填写有关含碳物质对应的性质
| 物质用途 | 金刚石切割玻璃 | 石墨作电极 | 活性炭净水 |
| 对应性质 |
|
|
|
(2)液态二氧化碳可用于扑灭珍贵的档案材料及电器火灾,下列说法错误的是
A、CO2不燃烧也不支持燃烧 B、液态CO2气化后不会损坏档案材料及电器
C、液态CO2是混合物 D、液态CO2中碳元素的化合价是+4价
(3)过多的二氧化碳会加剧“温室效应”,写一条减少二氧化碳排放的建议 .
(4)二氧化碳是一种宝贵的自然资源,利用二氧化碳、氨气和水可以制造化肥碳酸氢铵.该反应的化学方程式为 .
(5)石墨在一定条件下可以转化成金刚石,这一变化属于 (填化学变化或物理变化)
查看答案和解析>>
科目:初中化学 来源: 题型:
在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表.则关于此反应的说法正确的是( )
| 物 质 | X | Y | Z | W |
| 反应前的质量(g) | 2 | 1 | 16 | 16 |
| 反应后的质量(g) | 12 | m | 8 | 14 |
|
| A. | 物质Y一定是该反应的催化剂 | B. | 该反应的基本类型为分解反应 |
|
| C. | 参加反应的Z与W的质量比为4:1 | D. | 反应后生成X的质量为12 g |
查看答案和解析>>
科目:初中化学 来源: 题型:
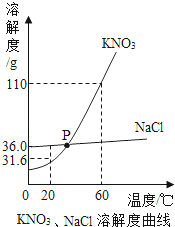
如图是KNO3、NaCl的溶解度曲线,如表是它们在不同温度时的溶解度.
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| KNO3/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| NaCl/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.8 |
(1)以上两种物质溶解度的变化受温度影响较小的是 .
(2)硝酸钾溶液中的溶剂是 .
(3)20℃时,KNO3的溶解度是 g.
(4)农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种.完成此溶液的配制正确的操作顺序是 (填序号).
①溶解 ②称量 ③计算 ④量取
(5)下列关于P点的理解正确的是 .
A.t℃时他们的溶解度相同
B.t℃时他们的溶液溶质质量分数一定相同
C.t℃时配制二者的饱和溶液,溶质质量分数一定相同.
查看答案和解析>>
科目:初中化学 来源: 题型:
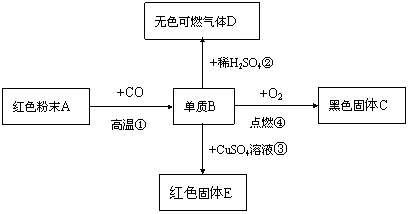
单质B是一种常见且用途广泛的金属,B元素在地壳中含量仅次于铝,已知金属B能发生如下一系列变化:
试推断:
(1)写出A—E的名称:A.___ B._____ C.______ D.______ E._____ ___。
(2)写出①—④各步反应的化学方程式:
①___________;②_______ ③_____④ _______
查看答案和解析>>
科目:初中化学 来源: 题型:
水是人类生活中不可缺少的物质。
(1)下列净水方法中,通常用于除去水中难溶性杂质的是_____,净水程度最高的是_____
A.过滤 B.煮沸 C.蒸馏 D.吸附
(2)自来水厂常用二氧化氯(ClO2)消毒,其中氯元素的化合价为________;
 (3)自来水中含有少量Ca(HCO3)2等可溶性化合物,烧水时Ca(HCO3)2发生分解反应,生成难溶性的碳酸钙、水和二氧化碳,这就是壶中出现水垢的原因之一。请写出Ca(HCO3)2受热分解的化学方程式_______________________。
(3)自来水中含有少量Ca(HCO3)2等可溶性化合物,烧水时Ca(HCO3)2发生分解反应,生成难溶性的碳酸钙、水和二氧化碳,这就是壶中出现水垢的原因之一。请写出Ca(HCO3)2受热分解的化学方程式_______________________。
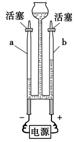
(4)为了探究水的组成,实验装置如右图所示
①该实验中,与两个电极相连的a、b两支玻璃管中产生的气体分别是
和 ,质量比为 。②写出该反应的化学方程式
(5)硬水给 生活和生产带来很多麻烦,生活中常用 区分硬水和软水,常用 方法降低水的硬度.
生活和生产带来很多麻烦,生活中常用 区分硬水和软水,常用 方法降低水的硬度.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com