
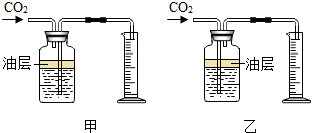
 化学兴趣小组测定某石灰石样品中碳酸钙的质量分数(假定:石灰石样品中除碳酸钙外,其余物质不与稀盐酸反应也不溶于水).
化学兴趣小组测定某石灰石样品中碳酸钙的质量分数(假定:石灰石样品中除碳酸钙外,其余物质不与稀盐酸反应也不溶于水).分析 (1)根据二氧化碳的性质、装置的特点来完成该题的解答;
(2)根据密度公式可以求算出二氧化碳气体的质量;然后结合碳酸钙与稀盐酸反应的化学方程式可以求得碳酸钙的质量,进而求算出碳酸钙的质量分数;
解答 解:Ⅱ(1)二氧化碳能够溶于水,所以为了使实验结果更准确,二氧化碳不能和水接触,所以应该选择甲装置,进入量筒中的水的体积即为二氧化碳的体积,而装置中油的作用就是为了防止二氧化碳溶于水而影响实验结果的;
(2)根据题意可知生成二氧化碳气体的体积为440mL=0.44L,所以根据密度公式可以知道生成二氧化碳气体的质量为:m=ρV=2.0g/L×0.44L=0.88g;
设石灰石样品中CaCO3的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 0.88g
$\frac{100}{44}=\frac{x}{0.88g}$ 解得:x=2.0g
该石灰石样品中CaCO3的质量分数为:$\frac{2.0g}{3.0g}$×100%=66.7%;
答案为:(1)甲,体积,防止二氧化碳气体溶于水;(2)该石灰石样品中CaCO3的质量分数为66.7%;
点评 熟练掌握二氧化碳及碳酸钙的化学性质,并记住相应的化学方程式,能够根据化学方程式进行简单的计算,另外要掌握质量分数的公式.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
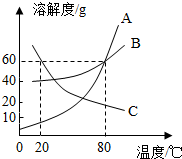 如图为A、B、C三种物质的溶解度曲线,据图回答:
如图为A、B、C三种物质的溶解度曲线,据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 人体中含量最多的金属元素是Ca | |
| B. | 日常生活中应用最广泛,目前世界上产量最高的金属是Fe | |
| C. | 地壳中含量最多的金属元素是Fe | |
| D. | 导电性最好的金属是Ag |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用一氧化碳还原氧化铜:CO+CuO$\frac{\underline{\;△\;}}{\;}$Cu+CO2(置换反应) | |
| B. | 铁与盐酸反应:2Fe+6HCl═2FeCl3+3H2↑(置换反应) | |
| C. | 盐酸与氢氧化铜反应:Cu(OH)2+2HCl═CuCl2+2H2O(复分解反应) | |
| D. | 将氯化钡溶液滴入硫酸铜溶液:CuSO4+BaCl2═BaSO4+CuCl2(复分解反应) |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
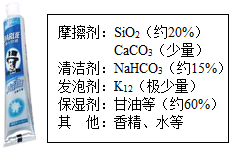 牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题.
牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题.| 实验编号 | 1 | 2 | 3 |
| 实验前/g | 2.00 | 2.00 | 2.00 |
| 实验后/g | 0.43 | 0.44 | 0.45 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
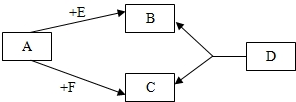 已知A、E、F是单质,B、C、D是化合物,都是初中常见的物质,它们分别是由碳、氢、氧三种元素中的一种或者几种组成.其中B是相对分子质量最小的氧化物,D物质很不稳定,容易分解生成B和C,它们之间的转化关系如图所示.
已知A、E、F是单质,B、C、D是化合物,都是初中常见的物质,它们分别是由碳、氢、氧三种元素中的一种或者几种组成.其中B是相对分子质量最小的氧化物,D物质很不稳定,容易分解生成B和C,它们之间的转化关系如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com