
| A. | 柠檬2.2~2.4 | B. | 鸡蛋清7.6~8.0 | C. | 西红柿4.0~4.4 | D. | 年奶6.3~6.6 |
科目:初中化学 来源: 题型:选择题
| A. | 二氧化碳:用于灭火 | B. | 明矾:用于净水 | ||
| C. | 烧碱:用于食用碱 | D. | 氯化钠:用于配制生理盐水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
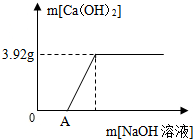 某环保小组监测到一工厂向河水中排放的酸性废液中含有CuSO4.
某环保小组监测到一工厂向河水中排放的酸性废液中含有CuSO4.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 把浓硫酸注入盛有水的量筒内稀释 | B. | 用镊子取用块状固体药品 | ||
| C. | 将pH试纸浸入待测液中测定pH | D. | 将实验剩余的药品放回原试剂瓶中 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
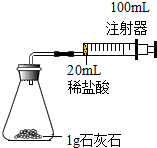 某化学实验小组对“影响石灰石与盐酸反应速率的因素-盐酸的浓度和石灰石的颗粒大小等”进行了如下实验探究,请你参与:
某化学实验小组对“影响石灰石与盐酸反应速率的因素-盐酸的浓度和石灰石的颗粒大小等”进行了如下实验探究,请你参与:| 实验编号 | 盐酸溶质质量分数(均取20ml) | 石灰石固体性质(均取1g) | 二氧化碳体积(ml)(均收集前30s的气体) |
| a | 4% | 颗粒 | 64.0 |
| b | 4% | 块状 | 40.4 |
| c | 6% | 颗粒 | 98.2 |
| d | 6% | 块状 | 65.3 |
| 时间/s | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 | 36 | 40 |
| 气体体积/ml | 16.0 | 22.2 | 29.4 | 39.3 | 50.4 | 57.6 | 62.0 | 64.7 | 66.0 | 66.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
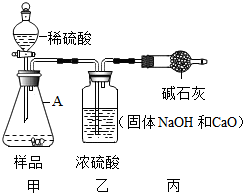 实验室贮存的烧碱易变质,围绕变质问题某学习小组同学取实验室放置了一段时间的烧碱固体样品进行下列探究,过程如下,请回答相关问题:
实验室贮存的烧碱易变质,围绕变质问题某学习小组同学取实验室放置了一段时间的烧碱固体样品进行下列探究,过程如下,请回答相关问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
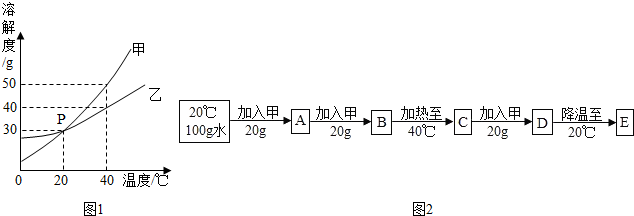
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com