
分析 由题目的信息可知,属于青嵩素化学性质的是:②可以与盐酸羟胺发生反应,产物遇铁离子显色;③青嵩素在60度以上时会完全分解;青嵩素的化学式是C15H22O5,则青嵩素中碳元素和氢元素的质量比C:H=(12×15):(1×22)=90:11;青嵩素的对抗病原体的作用机制是:青嵩素的作用机制主要是干扰疟原虫的细胞膜的合成,而使其很快死亡;灭蚊子是属于消灭虫媒传播,小明认为也可以通过煮熟青嵩,服用其汤汁的方法来治疗疟疾,我认为这种方法不可行,因为青嵩素在60度以上时会完全分解.
解答 解:(1)属于青嵩素化学性质的是:②可以与盐酸羟胺发生反应,产物遇铁离子显色;③青嵩素在60度以上时会完全分解;故答案为:②③;
(2)青嵩素的化学式是C15H22O5,则青嵩素中碳元素和氢元素的质量比C:H=(12×15):(1×22)=90:11;故答案为:90:11;
(3)青嵩素的对抗病原体的作用机制是:青嵩素的作用机制主要是干扰疟原虫的细胞膜的合成,而使其很快死亡;故答案为:青嵩素的作用机制主要是干扰疟原虫的细胞膜的合成,而使其很快死亡;
(4)灭蚊子是属于消灭虫媒传播,故答案为:消灭虫媒传播;
(5)小明认为也可以通过煮熟青嵩,服用其汤汁的方法来治疗疟疾,我认为这种方法不可行,因为青嵩素在60度以上时会完全分解;故答案为:不可行,因为青嵩素在60度以上时会完全分解;
点评 本考点考查了物理性质和化学性质的区分,要记忆有关青蒿素的性质,并能够在比较的基础上进行应用,本考点的基础性比较强,主要出现在选择题和填空题中.


科目:初中化学 来源: 题型:实验探究题
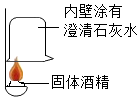 在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究.
在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究.| 方案 | 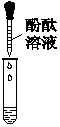 |  |
| 现象 | 溶液变红 | 产生白色沉淀 |
| 结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
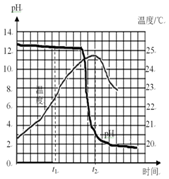 为研究酸和碱反应的特点,将稀盐酸匀速、缓慢地滴入盛有氢氧化钠溶液的烧杯中,并测绘出烧杯内溶液的温度和pH的变化图象(如图所示),请回答问题:
为研究酸和碱反应的特点,将稀盐酸匀速、缓慢地滴入盛有氢氧化钠溶液的烧杯中,并测绘出烧杯内溶液的温度和pH的变化图象(如图所示),请回答问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 将甲物质中逐渐加入乙物质至过量,若x轴表示加入乙物质的质量,则下列选项与如图相符合的是( )
将甲物质中逐渐加入乙物质至过量,若x轴表示加入乙物质的质量,则下列选项与如图相符合的是( ) | 选项 | 甲物质 | 乙物质 | Y轴表示的含义 |
| A | 碳酸钙 | 稀盐酸 | H2O的质量 |
| B | T℃的水 | 硝酸钾 | T℃硝酸钾的溶解度 |
| C | 铁与铜的混合粉末 | 硝酸铜 | 混合粉末中铜的质量 |
| D | 饱和石灰水 | 生石灰 | 溶液的质量 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 28.6% | B. | 25.6% | C. | 26.5% | D. | 40% |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
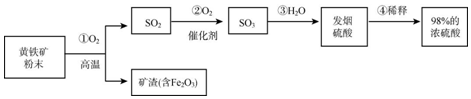
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
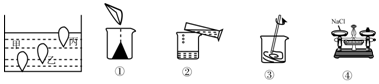
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com