
【题目】阅读下面科普短文。
[科普阅读理解]
柠檬酸广泛存在于植物中,如:柠檬、复盆子、葡萄等。因最初从柠檬果的汁中提出,故取名柠檬酸。19世纪末以来,主要用发酵法制取柠檬酸。我国以薯干等为原料,采用的深层发酵技术具有独创性,发酵指数居世界前列。
柠檬酸的化学式为 C6H8O7,又名枸橼酸,白色结晶性粉末,有很强的酸味,易溶于水,水溶液显酸性。0℃时,在100g水中最多可溶解133g。加热至175 ℃时它会分解产生二氧化碳和水,剩余一些白色晶体;与碱、甘油等发生反应。
柠檬酸在食品及卫生等方面具有广泛的用途。

柠檬酸粉
用于杀菌除垢
柠檬酸能与碳酸盐反应,因而能够快速分解附着在热胆内壁、饮水机、发热管、电水壶、蒸蛋器、茶壶等上的水垢。此外,柠檬酸还能杀灭细菌芽孢,具有很强的杀菌作用。某种含柠檬酸的除垢剂配方如图所示。
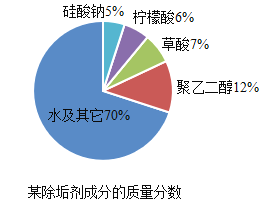
图1某除垢剂成分的质量分数
用于食品工业
柠檬酸有温和爽快的酸味,主要用作清凉饮料、果汁、果酱、水果糖和罐头等的酸性调味剂。同时可改善食品的感官性状,增强食欲和促进体内含磷等营养物质的消化吸收。
某种含柠檬酸的果冻的配料表如下(按100g计):
用料 | 果冻粉 | 白砂糖 | 牡丹花红色素 | 柠檬酸 | 草莓香精 |
用量 | 0.6 g | 17 g | 26 mg | 0.4 g | 0.17 g |
柠檬酸为可食用酸类,无论是用于食品工业还是杀菌除垢,适当剂量的柠檬酸对人体无害。但它可以促进体内钙的排泄和沉积,如长期食用含柠檬酸的食品,有可能导致低钙血症,对身体造成不良的影响。
依据文章内容回答下列问题。
(1)发酵法制取柠檬酸属于___________(填“物理”或“化学”)变化。
(2)柠檬酸中碳、氧元素的质量比为________。
(3)图1所示除垢剂中,柠檬酸所占的质量分数为_________。
(4)上述500g果冻中,含柠檬酸的质量是_____________g。
(5)下列说法正确的是___________(填字母序号)。
A、0℃时,柠檬酸在水中的溶解度是133g
B、只有从柠檬果中提取的柠檬酸,才能安全地食用
C、柠檬酸广泛应用于食品、卫生等领域
D、柠檬口味清爽,食用时多多益善
【答案】化学 9∶14 6% 2 AC
【解析】
(1)我国以薯干等为原料,采用深层发酵技术制取柠檬酸,有新物质生成,属于化学变化。
(2)根据柠檬酸的化学式C6H8O7,柠檬酸中碳、氧元素的质量比为:(12×6)∶(16×7)=9∶14。
(3)图1表示的是某除垢剂中各成分的质量分数。根据图示,该除垢剂中柠檬酸所占的质量分数为:6%。
(4)根据配料表提供的信息(注意:按100g计),上述500g果冻中,含柠檬酸的质量是:![]() 。
。
(5)A、根据阅读材料可知:0℃时,在100g水中最多可溶解133g。根据固体溶解度的含义,0℃时,柠檬酸在水中的溶解度是133 g,选项A正确;
B、我国以薯干等为原料制取的柠檬酸,也能安全地食用,选项B不正确;
C、根据题干提供的信息可知,柠檬酸在食品及卫生等方面具有广泛的用途,选项C正确;
D、根据题干提供的信息:柠檬酸为可食用酸类,用于食品工业,适当剂量的柠檬酸对人体无害,但它可以促进体内钙的排泄和沉积,如长期食用含柠檬酸的食品,有可能导致低钙血症,对身体造成不良的影响。因此虽然柠檬口味清爽,但要适量食用,选项D不正确。故正确的是AC。


 步步高达标卷系列答案
步步高达标卷系列答案科目:初中化学 来源: 题型:
【题目】如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线。
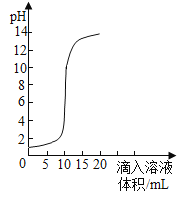
(1)氢氧化钠和盐酸恰好完全反应时,溶液的pH_____7(填“大于”或“小于”或“等于”)。
(2)根据曲线判断,该反应是将_____(填“氢氧化钠溶液”或“盐酸”)滴入另一种溶液中。
(3)当滴入溶液的体积为15mL时,所得溶液中的溶质为_____(写化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】地球深处的水处于超临界状态,称为超临界水。下图为某压强下CaCl2 和NaCl 在超临界水中的溶解度曲线,该压强下,下列说法正确是( )
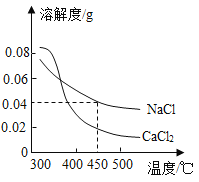
A.在超临界水中,NaCl的溶解度大于CaCl2的溶解度
B.在超临界水中,2种物质的溶解度都随温升高而增大
C.450℃时,NaCl在超临界水的溶解度为 0.04g
D.450℃时,可得到 0.04%的CaCl2的超临界水溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是钠元素和碘元素在元素周期表中的信息及粒子结构示意图,下列说法正确的是

A.钠和碘均为金属元素
B.钠原子和碘原子的最外层电子数之和为15
C.钠元素和碘元素形成化合物的化学式为Nal2
D.碘元素与氯元素化学性质相似,则碘化钠和氯化钠都是由离子构成的物质
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】取20.5g赤铁矿样品(主要成分为Fe2O3,杂质不溶于水,且不与酸反应)于烧杯中,逐渐加入稀硫酸充分反应。所加稀硫酸的质量与烧杯中剩余固体质量的关系如图所示。请计算:

(1)该样品中氧化铁的质量为____________g;
(2)恰好完全反应时,烧杯中溶液的溶质质量分数________。(请写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用下图装置研究CO2与NaOH溶液的反应。关闭止水夹K,将足量NaOH溶液挤进烧瓶,振荡,打开止水夹K,水倒吸入烧瓶,形成红色喷泉。
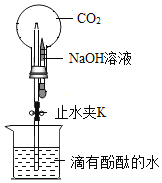
(1)CO2与NaOH发生反应的方程式为________。
(2)打开止水夹后,水倒吸入烧瓶的原因是_______。
(3)实验结束后,取下烧瓶,打开橡胶塞,向其中加入足量的稀盐酸,可能观察到的现象是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体物质的溶解度曲线如图所示。现将两支分别装有甲、乙两种物质的饱和溶液(底部均有未溶解的固体)的试管浸入盛有水的烧杯中(如图),然后向烧杯中加入一定量的浓硫酸。则对相关变化判断正确的是

A.甲溶液中溶质的质量分数增大
B.乙溶液中溶质的质量分数增大
C.甲、乙两种物质的溶解度都增大
D.甲溶液中未溶解的固体质量减少
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向一定量的氯化铜和氯化亚铁的混合溶液中逐渐加入过量的镁粉,如图表示反应过程中溶液中FeCl2的质量变化情况。
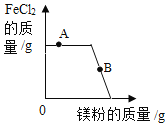
(1) A点时溶液中含有哪些溶质? (写化学式)_______________。
(2)写出B点时发生反应的化学方程式_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明和小红同学用打磨过的大小相同的铝片分别与pH相同的稀盐酸、稀硫酸反应(装置和现象记录如下图表格),请你与他们一起探究。
时间 | 1 | 2 | 5 | 15 | 20 |
稀盐酸现象 | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 反应结束 |
稀硫酸现象 | 无明显现象 | 无明显现象 | 极少量气泡 | 少量气泡 | 少量气泡 |
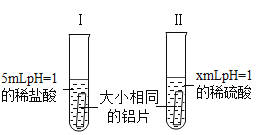
(1)实验中X的数值为_______________,写出铝与稀盐酸反应的化学方程式_______________。
(2) [提出问题]什么原因影响铝和稀盐酸和稀硫酸反应现象不同?
(3)[猜想假设]猜想一:________________对反应起了促进作用;猜想二:稀硫酸中的硫酸根离子对反应起了阻碍作用。
(4)[实验验证]为了验证哪个猜想正确,小明进行了如下实验:向试管II中加入少量____________ (填序号),向试管I中加入少量______________(填序号),做对比实验。
A硫酸铜 B氯化钠 C硫酸钠 D浓盐酸
通过对比实验,观察到_____________________现象,则猜想一成立。
(5) [反思评价]右图是小红将一根铝丝与过量的稀盐酸混合在一密闭容器内反应,利用压强和温度传感器测出的反应变化过程(上面是压强变化曲线、下面是温度变化曲线)。那么,在__________(填“A、 B、C、D”)点时铝与酸反应结束,请你解释压强曲线AB段、BC段、CD段变化原因。
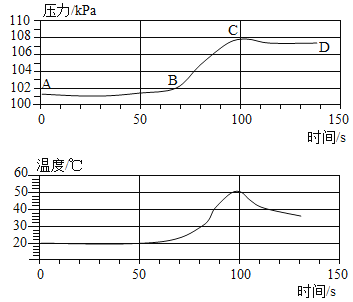
①____________________。
②_____________________。
③_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com