
(5分)化学自主学习小组同学实验探究氧化镁与稀盐酸反应后溶液中溶质成分。
【提出问题】氧化镁与稀盐酸反应后溶液B中含有的溶质是什么?
【猜想与假设】猜想一:MgCl2
猜想二:(1)______________
【进行实验】小组同学向溶液B中滴加氢氧化钠溶液,边滴加边搅拌,开始时无明显现象,继续滴加一段时间后出现白色沉淀。
【表达与交流】产生上述现象的原因是(2)_________________________________________________;当白色沉淀刚开始出现时,溶液中含有的离子是(3)______________(填离子符号)。
【解释与结论】猜想二成立。
【反思与评价】分析反应后溶液中溶质成分时,需要考虑的因素有(4)______________________。
(1)MgCl2、HCl(1分);(2)开始时加入的氢氧化钠溶液量少,与稀盐酸反应,生成氯化钠和水,无明显现象。待稀盐酸耗尽后,氢氧化钠与氯化镁反应,生成氢氧化镁出现白色沉淀。(2分) (合理即可);(3)Na+、Mg2+、Cl-(1分) ;(4)可溶的生成物和可溶的剩余的反应物(1分)(合理即可)
解析试题分析: (1)当盐酸有剩余时,所得溶液中的溶质为氯化镁MgCl2和氯化氢HCl;(2)开始加入氢氧化钠时无现象,说明溶液中有氯化氢存在,等氯化氢反应完后,氢氧化钠与氯化镁反应生成氢氧化镁白色沉淀;(3)当白色沉淀刚开始出现时,溶液中含有生成的氯化钠和没反应的氯化镁,离子符号为Na+、Mg2+、Cl-;(4)分析反应后所得溶液中的溶质,应考虑生成的可溶性物质及是否有剩余的可溶性的反应物。
考点: 科学探究;碱的性质


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:单选题
小李设计的以下实验方案中,可行的是( )
| A.用二氧化锰鉴别过氧化氢和蒸馏水 |
| B.用稀盐酸检验某黄金饰品中是否含有铜 |
| C.用闻气味的方法区别一氧化碳和二氧化碳气体 |
| D.用适量的氯化钡溶液除去硝酸钠溶液中的硫酸钠杂质 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2)。该维C泡腾片是 (填纯净物或混合物)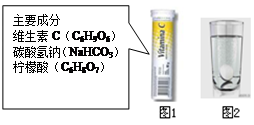
该小组同学对该气体的成分进行如下探究。
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、N2。
小明说:不可能含有N2,因为
_________________________________________。
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,而CO有剧毒。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
查看答案和解析>>
科目:初中化学 来源: 题型:问答题
(10分)某化学兴趣小组把金属钠投到硫酸铜溶液中,实验并非如、想象的有红色铜析出,
而是生成一种蓝色沉淀。同学们非常好奇并进行实验探究。
【提出问题)金属钠投到硫酸铜溶液中到底发生了怎样的化学反应?
【查阅资料】钠是非常活泼的金属,能跟氧气反应,也能与水发生剧烈反应,并放出气体,
生成的溶液显碱性。
【提出猜想】
猜想1:钠先与水反应生成氢气和某碱溶液,某碱再与硫酸铜反应生成蓝色沉淀:
猜想2:钠先与水反应生成氧气和某碱溶液,某碱再与硫酸铜反应生成蓝色沉淀。
【实验探究】实验一:同学们把一小块切干净的钠投到装有少量蒸馏水的试管中,观察到钠浮
在水面上,并产生气泡;点燃生成的气体,听到“噗”的一声后燃烧起来。
实验二:在剩余的溶液中加入硫酸铜溶液,发现有蓝色沉淀。
【实验分析】
(1)根据“实验一”判断,金属钠的密度比水 (填“大”或“小”);“实验一”中可以燃
烧的气体的化学式是 。
(2)两个猜想中的“某碱”是 ;金属钠与水反应的化学方程式是 。
(3)“实验二”中发生反应的化学方程式是 。
【实验结论】请你判断:猜想 成立。
【实验反思】金属钠通常保存在煤油中,目的是隔绝 和 。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
(7分)镁与NH4Cl溶液反应,不仅有一种盐生成,还有气泡产生。为确定气体的成分,进行下列实验探究。
(一)探究:气体可能是HCl、02、NH3、H2中的一种或几种。
(二)实验:
(1)甲同为确定是否含有HCl,他将气体通入酸化的硝酸银溶液中,无明显现象,则该气体中_ HCl (填“有”或“无”)。
(2)乙同学认为只有02,则可用_ 来检验。实验证明乙同学的观点不正确。
(3)丙同学为判断是否含有H2,同时确定气体成分,通过查阅资料得知:
2NH3+3CuO ="=" 3Cu+N2+3H20于是他设计了如下图实验装置:
(三)实验现象与结论:A中观察到_ ,证明有NH3; B中玻璃管内观察到_ ,证明有H2。
(四)实验反思:
(4)浓硫酸的作用是_ 。
(5)大家认为丙同学在加热之前,应对气体先_ 以确保安全。
(6)写出Mg与NH4Cl溶液反应的化学方程式 。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
定性和定量结合既是化学的重要思想,也是研究物质组成的重要方法。某研究性学习小组为检测实验室用H2还原CuO所得红色固体Cu中是否含有Cu2O(红色),进行了认真的研究。请你一起踏上探究之路,回答下列问题。
【查阅资料】①无水CuSO4遇水变蓝 ②高温灼烧CuO生成Cu2O和O2 ③Cu2O与稀H2SO4反应:Cu2O+H2SO4=Cu+CuSO4+H2O
【设计实验方案】
方案1 取该红色固体加入适量稀H2SO4,实验现象为 ,结论为红色固体中含有Cu2O.
方案2 装置如图所示,拟通过干燥管中CuSO4变蓝来判断红色固体是否含有Cu2O.
(1)为确保探究的科学、合理、安全.实验中还应采取的措施有 ;(填序号)
①加热前先排尽装置中的空气
②在氢气发生器与硬质玻璃管之间加一个干燥装置
③在盛有CuSO4的干燥管后再连接一个装有浓H2SO4的洗气瓶
(2)由方案2实验后得出结论:红色固体中含有Cu2O.写出红色固体Cu2O与H2反应的化学方程
式
方案3 称得干燥坩埚(常用于固体加热的容器)的质量为ag,取红色固体置于坩埚中称得总质量为bg,在空气中高温灼烧至质量恒定,称得最后坩埚与固体总质量为cg.
(1)该实验方案最少得进行 次称量;
(2)若确认红色固体中含有Cu2O,则c与a,b应符合的数学关系式为 .
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
化学课堂上要学习碱的化学性质,老师让两位同学和他共同做实验,要求两位同学分别向澄清石灰水和氢氧化钠溶液中吹气,如图①②所示,老师告诉同学们,呼出的气体中只有二氧化碳有可能与澄清石灰水和氢氧化钠溶液反应.
同学们在吹气后观察到①中澄清石灰水边浑浊,②中氢氧化钠溶液无明显现象.观察实验现象后老师问,通过实验现象的观察,检验二氧化碳气体应该使用 ,针对②中的情况,师生共同开始探究之旅.
【提出问题】二氧化碳通入氢氧化钠溶液中无明显现象,两者是否发生了化学反应?
【猜想假设】猜想A:两者发生了化学反应;猜想B:两者没有发生化学反应.
【实验探究】
(1)小明设计了如图所示的③、④两个实验.
实验现象:③中的软塑料瓶变瘪,④中 .
(2)小亮认为小明的实验是可行的,其共同原理是二氧化碳和氢氧化钠溶液反应,使容器内压强降低,小光同学却对此提出了质疑,他认为小明的实验不严谨,若仍利用该装置,需要补做的对比实验是 .
(3)小光设计的是通过检验生成物来验证猜想,请帮他填写实验报告:
| 实验步骤 | 实验现象 | 实验结论 |
| 取③实验后的溶液少许,再向其加入 ( ) | | 验证了二氧化碳和氢氧化钠溶液反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
(6分)某小组同学将BaCl2溶液与H2SO4溶液混合,将反应后的液体过滤,并探究滤液的成分,请你参与探究并回答相关问题。
【问题与发现】Ⅰ.BaCl2溶液与H2SO4溶液混合,发生反应的化学方程式是: 。
Ⅱ.滤液里的溶质是什么?
【猜想与假设】
猜想1:滤液里的溶质只有HCl;
猜想2:滤液里的溶质有HCl和H2SO4;
猜想3:滤液里的溶质有HCl和 。
【探究与验证】
| | 实验操作 | 现 象 | 结 论 |
| 甲 | 取少量滤液,加入少量锌粒 | 有气泡产生 | 猜想2成立 |
| 乙 | 取少量滤液,加入少量的Na2SO4溶液 | | 猜想3成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
(5分)某实验小组利用如图所示装置测量空气中氧气体积分数并取得成功。
【查阅资料】白磷的着火点40℃。
【提出问题】氧气体积约占空气总体积的多少?
【实验准备】锥形瓶内空气体积为230mL,注射器中水的体积为50mL,该装置气密性良好。
【实验探究】装入药品,按图所示连接好仪器,夹紧弹簧夹。先将锥形瓶底部放入热水中,白磷很快被引燃,然后将锥形瓶从热水中取出。
【现象分析】
(1)将锥形瓶底部放入热水中,白磷被引燃,说明燃烧不能缺少的一个条件是____________________,写出白磷燃烧的化学方程式:______________________________。
(2)在整个实验过程中,可观察到气球的变化是___________________。
(3)待白磷熄灭、锥形瓶冷却到室温后,打开弹簧夹,还可观察到的现象是:①注射器中的水自动喷射出来,②当注射器中的水还剩约4mL时停止下流。导致这些现象发生的原因是:__________________。
【得出结论】氧气约占空气总体积的1/5 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com