
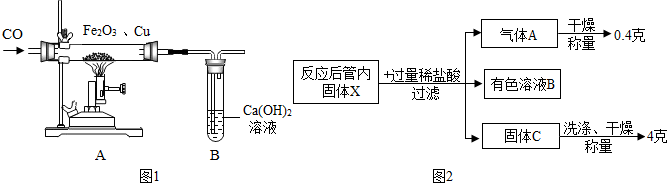
分析 根据一氧化碳还原氧化铁的步骤、注意事项解答;根据金属与酸反应规律、酸的化学性质及化学方程式进行计算分析解答.
解答 解:(1)一氧化碳具有可燃性,点燃时会可能发生爆炸,实验时要“先通一氧化碳气体,后加热”目的是排尽玻璃管内的空气,防止加热时发生爆炸;
(2)一氧化碳还原氧化铁生成铁和二氧化碳,化学方程式为3CO+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
(3)实验装置B中二氧化碳通入石灰水中,现象是 澄清石灰水变浑浊;发生反应的化学方程式CO2+Ca(OH)2═CaCO3↓+H20
(4)一氧化碳有剧毒,不能直接排放到空气中,故需将尾气点燃或用气球收集起来.
(5)铁与盐酸反应生成氯化亚铁和氢气,方程式为Fe+2HCl═FeCl2+H2↑;
(6)反应后管内固体是铁和铜的混合物,加入过量盐酸后,铁与盐酸反应产生氢气,根据氢气的质量可求出铁的质量,根据铁元素的质量可求出氧化铁的质量.反应后溶液中的溶质是铁与盐酸反应生成的氯化亚铁和剩余的盐酸,固体C是铜,表面残留着盐酸,故可取最后的洗涤液滴加紫色石蕊试液,看是否变红确定是否洗涤干净.
(7)设铁的质量为x,
Fe+2HCl═FeCl2+H2↑
56 2
x 0.4g
$\frac{56}{x}$=$\frac{2}{0.4g}$
x=11.2g
所以氧化铁的质量为 $\frac{11.2g×160}{112}$=16g,
所以原混合物“氧化铁和铜粉”中铜的质量分数为$\frac{4g}{4g+16g}$×100%=20%
故答案为:(1)排尽玻璃管内的空气,防止加热时发生爆炸
(2)3CO+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
(3)石灰水变浑浊CO2+Ca(OH)2═CaCO3↓+H20
(4)将尾气点燃或用气球收集
(5)Fe+2HCl═FeCl2+H2↑
(6)取最后的洗涤液滴加紫色石蕊试液,看是否变红,若不变红,说明已洗干净.
(7)4.
点评 化学反应前后元素质量守恒,根据铁元素质量守恒可求出氧化铁质量,进而求出铜的质量分数.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 马踏飞燕(青铜器) | B. | 龙泉剑(铁器) | C. | 金缕衣 | D. | 米酒 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 项目 | 标准 |
| 感官指标 | 无异味、异臭等 |
| 化学指标 | pH6.5-8.5,铜<1.0mg•L-1,铁<0.3mg•L-1,氟化物<1.0mg•L-1,游离氯≥0.3mg•L-1等 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com