
科目:初中化学 来源: 题型:选择题
| A. | NaCl HCl MgSO4 Cu(NO3)2 | |
| B. | AgNO3 NaCl Mg(NO3)2 NaOH | |
| C. | Ca(OH)2 NaNO3 Na2CO3 NH4Cl | |
| D. | HCl K2SO4 NaOH NaNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 事 实 | 解释 |
| A | 品红在热水中扩散得更快 | 温度升高,分子能量增大,运动速率加快 |
| B | 液化石油气经过加压后压缩至到钢瓶中 | 气体分子间有间隔,且间隔较大 |
| C | 冰水混合物属于纯净物 | 冰、水由同种分子构成 |
| D | 酸、碱、盐的水溶液都能导电 | 溶液中有自由移动的带负电的电子 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 温度/℃ | 0 | 40 | 80 |
| Ca(OH)2溶解度/g | 0.187 | 0.141 | 0.094 |
| Ba(OH)2溶解度/g | 1.67 | 8.22 | 101.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 熟石灰 | B. | 稀盐酸 | C. | 硫酸铜 | D. | 二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 添加大量的亚硝酸钠来保鲜食品 | B. | 道路积雪可撒食盐以促进冰雪融化 | ||
| C. | 农业上常用硫酸铜配制波尔多液 | D. | 用纯碱除去面粉发酵生成的酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 有氧气(或空气) | B. | 有可燃物 | ||
| C. | 温度达到着火点 | D. | 同时满足以上三个 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 熔点 | 沸点 | 热稳定性 | 其他 |
| 101℃~102℃ | 150℃~160℃升华 | 100.1℃分解出水,175℃分解成CO2、CO、H2O | 与 Ca(OH)2反应产生白色沉淀(CaC2O4) |

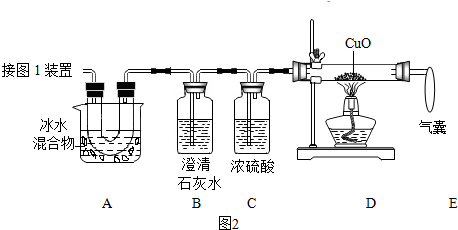
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com