解:
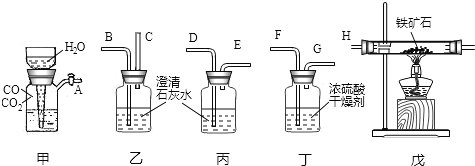
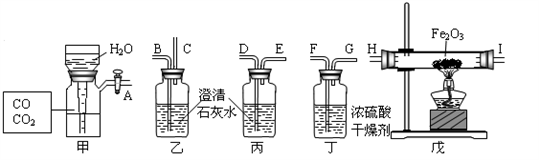
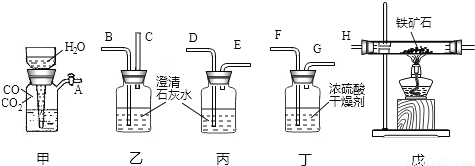
(1)得到纯净干燥的一氧化碳应先纯净后干燥.
(2)澄清石灰水的作用有检验二氧化碳和吸收二氧化碳两个作用.
(3)一氧化碳还原铁矿石的步骤是实验开始先通CO,实验结束时还要通一会CO.
(4)根据化学方程式中生成物CO
2的质量可求出反应物Fe
3O
4的质量
(5)一氧化碳有剧毒,不能直接排放到空气中,可用点燃法除去.
故答案为(1)A、D、E、F、G、H、I、B
(2)证明并吸收反应生成CO
2.除去混在CO中的CO
2(3)防止CO与空气混合加热后爆鸣或爆炸
(4)80%
(5)缺少尾气处理装置;在C处放一盏燃着的酒精灯.
分析:(1)要得到纯净干燥的一氧化碳,首先要通过澄清石灰水除去一氧化碳中的二氧化碳,然后通过浓硫酸除去一氧化碳中的水分,因此装置连接顺序应是A、D、E、F、G、H、I、B.
(2)装置乙和丙中都盛有澄清石灰水,但乙和丙装置的不同点在于C和E,E导管可以连接下一个装置将气体导入,故丙装置是用来除去一氧化碳中二氧化碳的,乙装置是用来检验并吸收二氧化碳的.
(3)一氧化碳具有可燃性,加热或点然一氧化碳与空气的混合物可能发生爆炸,因此CO还原四氧化三铁实验开始时要先通一会一氧化碳,排净装置内的空气.
(4)乙装置增加的1.76g是生成的二氧化碳的质量,根据一氧化碳还原四氧化三铁的化学方程式
4CO+Fe
3O
4
3Fe+4CO
2根据二氧化碳的质量可求出四氧化三铁的质量为2.32g,进而求出铁矿石中四氧化三铁的质量分数为80%.
(5)因为一氧化碳还原四氧化三铁实验结束时还要继续通一氧化碳直到玻璃管冷却,一氧化碳有剧毒,不能直接排放到空气中,因此装置中需要有尾气处理装置,防止逸散到空气中污染空气.
点评:本题是一道综合实验题,关健是搞清实验原理及每一装置及试剂的作用,连接好实验装置.

 3Fe+4CO2根据二氧化碳的质量可求出四氧化三铁的质量为2.32g,进而求出铁矿石中四氧化三铁的质量分数为80%.
3Fe+4CO2根据二氧化碳的质量可求出四氧化三铁的质量为2.32g,进而求出铁矿石中四氧化三铁的质量分数为80%.