
 铝箔是现代生活中常见的包装材料,放置久了,其白色光泽会变暗淡,故又称假银箔.
铝箔是现代生活中常见的包装材料,放置久了,其白色光泽会变暗淡,故又称假银箔.分析 (1)根据铝的性质、溶液的浓度逐渐降低分析回答;
(2)由于铝与稀盐酸反应放出了氢气,减少的质量就是生成的氢气的质量,由氢气的质量求出铝的质量再计算出样品中单质铝的质量分数.
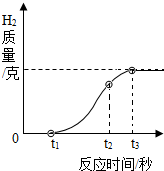
解答 解:(1)0~t1时间段内,铝箔表面看不到明显的气泡,原因是:铝在空气中被氧气氧化,生成一层致密的氧化铝保护膜,阻止铝与稀盐酸反应;t2~t3时间段产生气泡速度放缓的原因是稀盐酸的溶质质量分数在反应中逐渐降低;
(2)生成氢气的质量3.8g+100g-103.4g=0.4g
设生成0.4克氢气,需要参加反应的单质铝的质量为x
2Al+6HCl═2AlCl3+3H2↑
54 6
x 0.4g
$\frac{54}{x}$=$\frac{6}{0.4g}$
x=3.6g
单质铝的质量分数:$\frac{3.6g}{3.8g}$×100%≈94.7%
故答案为:(1)铝在空气中被氧气氧化,生成一层致密的氧化铝保护膜,阻止铝与稀盐酸反应;稀盐酸的溶质质量分数在反应中逐渐降低;
(2)94.7%.
点评 本题属于根据化学方程式的简单计算,难度不大,掌握铝的性质、根据化学方程式计算的方法即可分析回答.


科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象、结论 |
| 将产生的气体通入澄清石灰水中 | 若澄清石灰水变浑浊,则说明产生的气体为二氧化碳气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaOH Na2CO3 H2SO4 | B. | NaCl Na2SO4 NaOH | ||
| C. | NaCl Ba(NO3)2 K2SO4 | D. | CuSO4 Na2SO4 NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作步骤 | 实验现象 | 结论及解释 |
| 步骤一:取少量固体样品于试管中,加蒸馏水完全溶解,然后加入足量的稀盐酸. | 实验过程中始终没有气泡产生. | 则证明猜想Ⅰ成立. |
| 步骤二:另取少量固体样品于试管中,加蒸馏水完全溶解,然后滴加氯化钡溶液. | 实验过程中产生白色沉淀. | 则证明猜想Ⅱ或Ⅲ成立. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
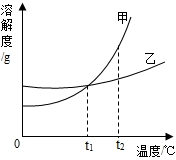 甲、乙两种固体的溶解度曲线如图所示.下列有关叙述中错误的是( )
甲、乙两种固体的溶解度曲线如图所示.下列有关叙述中错误的是( )| A. | t2℃时甲的溶解度比乙大 | |
| B. | 将相等质量的甲、乙两物质的饱和溶液温度从t2℃降到t1℃,析出的甲固体质量比乙固体质量大 | |
| C. | 升高温度可将甲的饱和溶液变为不饱和溶液 | |
| D. | t2℃时,甲和乙的饱和溶液各100g,其中溶质的质量相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com