
分析 (1)根据盐酸与氢氧化钙反应的现象考虑;
(2)根据对照实验的设计方法考虑;
(3)根据化学方程式的书写方法考虑;
(4)根据氢氧化钙与硫酸铜能产生蓝色沉淀考虑.
解答 解:(1)盐酸与氢氧化钙反应生成氯化钙和水,没有现象,所以方案一不行;
(2)对照实验的设计方法:加入盐酸和加入蒸馏水进行对照,得出结论,所以分别加入5mL浓度为5%的稀盐酸和5mL蒸馏水进行实验;
(3)反应物是氢氧化钙和盐酸,生成物是氯化钙和水,用观察法配平,所以化学方程式表示为:Ca(OH)2+2HCl=CaCl2+2H2O;
(4)氢氧化钙与硫酸铜能产生蓝色沉淀,如果加入硫酸铜后,没有生成蓝色沉淀,说明氢氧化钙与盐酸发生了反应.
故答案为:(1)盐酸与氢氧化钙反应生成氯化钙和水,无明显现象;
(2)蒸馏水;
(3)Ca(OH)2+2HCl=CaCl2+2H2O;
(4)无明显现象.
点评 本题考查了常见反应的设计及评价,解答本题关键是知道氢氧化钙与盐酸反应后无明显现象.


科目:初中化学 来源: 题型:解答题
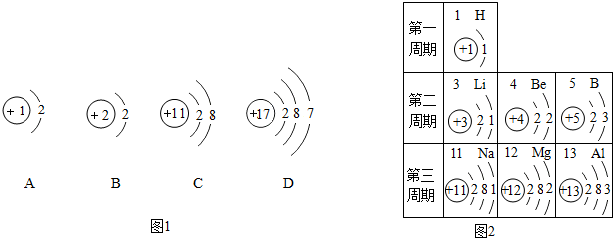
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
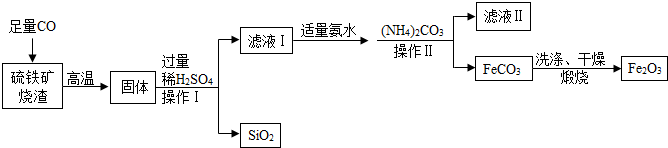
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用CO2来区分两种无色液体:水和石灰水 | |
| B. | 用点燃的方法除去CO2中混有少量CO | |
| C. | 用灼烧的方法区分两种黑色粉末:木炭粉和氧化铜 | |
| D. | 用过滤的方法除去NaCl溶液中混有的少量大理石 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 物 质 | Cu(OH)2 | Fe (OH)3 |
| 开始沉淀pH | 4.2 | 1.2 |
| 完全沉淀pH | 6.7 | 3.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com