
钨酸(H2WO4)中钨元素的化合价为
A. +2 B. +3 C. +4 D. +6
D 【解析】根据在化合物中正负化合价代数和为零,氢元素显+1,氧元素显-2,设钨元素的化合价是x,可知钨酸(H2WO4)中钨元素的化合价为(+1×2)+x+(-2)×4=0,则x=+6。故选D。 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:初中化学 来源:内蒙古乌拉特前旗2018届九年级第一模拟考试化学试卷 题型:推断题
某化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙,设计实验方案如下,请参与实验并回答问题。
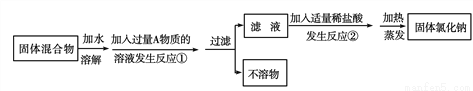
(1)写出A物质的化学式_____________,写出A物质的俗称_____________。
(2)写出反应②的化学方程式_________________________________________。
(3)反应①中加入过量A物质的目的是_________________________________。
反应②中如果加入盐酸也过量,则对所得到的氯化钠纯度________ (填“有”或“没有”)影响。
(4)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果________ (填“增大”、“不变”或“减小”),其原因是_______________;你认为加入适量盐酸应依据的现象是_______________。
Na2CO3 纯碱 Na2CO3+2HCl===2NaCl+H2O+CO2↑ 使氯化钙完全反应(合理即可) 没有 增大 加入过量的碳酸钠与盐酸反应也生成氯化钠 滤液中无气泡产生 【解析】本题考查了化学实验方案设计与评价,酸、盐的性质,化学方程式的书写。认真分析,根据条件综合把握化学反应。 (1)要除去氯化钠中的少量杂质氯化钙,只要除去钙离子就可以了,氯离子不是杂质。因此可以加入足量是碳...查看答案和解析>>
科目:初中化学 来源:广东省江门市2018届九年级下学期第二次模拟考试化学试卷 题型:填空题
根据下表信息,完成表中空格:
化学符号 | ______ | ______ | 3H2 | ______ |
符号的意义 | 4个硫原子 | 铝离子 | ______ | 空气中体积分数最大的物质 |
查看答案和解析>>
科目:初中化学 来源:福建省福州市2018届九年级5月质量检测化学试卷 题型:简答题
工业上将氯化钠转化为氯酸钾(KClO3)晶体的简易流程如图所示:
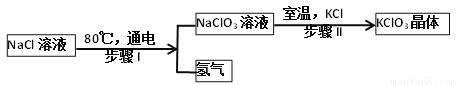
⑴ 步骤I反应的化学方程式为______________________。
⑵ 步骤II析出晶体后的溶液是KClO3的______(填“饱和溶液”或“不饱和溶液”)。
⑶ 下图分别为固体氯化钠和氯化钾的溶解度曲线。
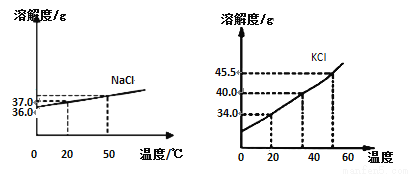
①医用生理盐水为0.9%的氯化钠溶液,该溶液可为人体补充的营养素有________。
②60℃时,10 g水中最多溶解氯化钾的质量为_____g。氯化钠和氯化钾在某一温度时,具有相同的溶解度,据图11所示,则该温度(t)的范围是_________。
③ 若采用某氯化钠溶液来选种,氯化钠与水的质量比为9︰41。将配制好的溶液装入试剂瓶,贴上标签,在下图中注明标签上的内容。
 ________________
________________
查看答案和解析>>
科目:初中化学 来源:福建省福州市2018届九年级5月质量检测化学试卷 题型:单选题
2017年5月9日,中科院发布了四种新元素的中文名称(如下表)。下列说法正确的是
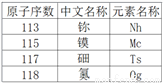
A. 四种元素都属于金属元素
B. “Nh”可表示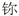 单质
单质
C. Og是地壳中含量最多元素
D. 镆原子的相对原子质量是115
B 【解析】A、由题中信息可知,117号元素带有“石字旁”,118号元素带有“气字头”,都不属于金属元素,错误;B、“Nh”可表示鉨单质,正确;C、地壳中含量最多元素是氧元素,错误;D、镆原子的质子数=核电荷数=核外电子数=原子序数=115,错误。故选B。查看答案和解析>>
科目:初中化学 来源:山东省潍坊市寿光、高密市2018届初三一模化学试卷 题型:综合题
酸、碱、盐在生产生活中具有广泛的用途。
(1)制作“叶脉书签”需用到10%的氢氧化钠溶液。现配制100g质量分数为10%的氢氧化钠溶液。
①若用氢氧化钠固体配制,需称量氢氧化钠的质量为__________g。
②用氢氧化钠固体配制10%的氢氧化钠溶液过程中,需要用到的仪器除了托盘天平、药匙、烧杯、玻璃棒、胶头滴管、试剂瓶外,还需要__________。
③下列操作正确的是__________(填字母序号)。
A.称量氢氧化钠固体时,左盘放砝码
B.在托盘天平的左右托盘上垫滤纸称量氢氧化钠固体
C.将准确称量的氢氧化钠固体放入装有水的量筒中溶解
D.将配好的氢氧化钠溶液装入试剂瓶中,塞好瓶塞并贴上标签
④若用20%的氢氧化钠溶液加水(水的密度为1g/cm3)配制100g质量分数为10%的氢氧化钠溶液,需20%的氢氧化钠溶液的质量为_________g;配制时应选用_________mL的量筒取水(填“100”或“50”或10)。
(2)某固体粉末可能含有碳酸钙、硫酸钠、氯化钠、氯化钡、硫酸铜中的一种或几种。为确定该固体粉末的成分,进行了如下实验:

回答下列问题:
①反应Ⅰ的化学方程式为__________________________。
②白色沉淀C是_________________(填化学式)。
③原固体粉末中一定不含________________、______________(填化学式)。
10 量筒 D 50 50 CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ BaSO4 CuSO4 BaCl2 【解析】(1)①需要氢氧化钠固体的质量=100g×10%=10g;②用氢氧化钠固体配制10%的氢氧化钠溶液过程中,需要用到的仪器除了托盘天平、药匙、烧杯、玻璃棒、胶头滴管、试剂瓶外,还需要量筒;③A、称量氢氧化钠固体时,应该砝码放在右盘,氢氧化钠放在左边,错误;...查看答案和解析>>
科目:初中化学 来源:山东省潍坊市寿光、高密市2018届初三一模化学试卷 题型:单选题
如图为甲、乙两种固体物质(不考虑结晶水)的溶解度曲线,下列说法错误的是( )

A. 20℃时,甲、乙具有相同的溶解度
B. 甲、乙的溶解度都随温度的升高而增大
C. 20℃时,可以配制溶质的质量分数为25%的甲溶液
D. 50℃时,甲和乙各30g分别加入100g水中,充分溶解后同时等速降温,则乙溶液先有固体析出
C 【解析】A.20 ℃时,甲、乙的溶解度相等,正确;B.甲、乙的溶解度都随温度的升高而增大,正确;C.20 ℃时,甲的溶解度是25g,形成的饱和溶液中溶质的质量分数为:×100%=20%,不能配制溶质的质量分数为25%的甲溶液,错误;D.20 ℃--50℃的某一温度,甲的溶解度大于乙的溶解度,故50℃时,甲和乙各30g分别加入100g水中,充分溶解后同时等速降温,则乙溶液中先有固体出现,正...查看答案和解析>>
科目:初中化学 来源:重庆市2018届九年级上学期期末考试化学试卷 题型:计算题
硫酸亚铁(FeSO4)常用来作补血剂,绿矾(FeSO4·7H2O)又是一种重要的食品和饲料添加剂。实验室用铁与稀硫酸反应既可以制得硫酸亚铁,也可以制得绿矾。
(1)计算7.6g硫酸亚铁中铁元素的质量___________。
(2)阅读下边的信息提示,列式计算FeSO4·7H2O的相对分子质量__________。

(3)将6g生铁渣加在装有足量稀硫酸的烧杯中,充分反应后,烧杯中物质的总质量减少了0.2g,计算:
①生成硫酸亚铁的质量_________。
②生铁中铁的质量分数____________。
2.8g (56+32+16×4) +7×(1×2+16)=278 15.2 93.3% 【解析】本题考查了相对分子质量的概念及其计算,根据化学反应方程式的计算,化合物中某元素的质量计算 (1)7.6克硫酸亚铁中铁元素的质量为:7.6g× ×100%=2.8g, (2)FeSO4•7H2O的相对分子质量为:(56+32+16×4)+7×(1×2+16)=278, (3)①设...查看答案和解析>>
科目:初中化学 来源:海南省琼海市2018届九年级中考模拟考试(一)化学试卷 题型:实验题
某同学在课外阅读中得知:实验室用电石(主要成分CaC2)与水反应制取乙炔(C2H2)反应的方程式为CaC2+2H2O=Ca(OH)2+C2H2↑。在实验室中该同学把一定量的CaC2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液,并对滤液的成分进行探究。
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】猜想一:NaOH
猜想二:NaOH,Ca(OH)2
猜想三:NaOH,Na2CO3
【设计并实验】
实验 | 实验操作 | 实验现象 | 实验结论 |
实验一 | 取少量滤液于试管中,向试管这滴入适量的碳酸钠溶液 | 猜想二不成立 | |
实验二 | 另取少量滤液于试管中,向其中加入过量稀盐酸 | 产生气泡 | 猜想 成立 |
写出实验二中产生气泡的化学方程式:
【拓展延伸】
①若向Cu(NO3)2溶液中加少量CaC2,充分反应,产生的现象是 。
②实验室保存电石应注意 。
【设计并实验】无白色沉淀生成 三 Na2CO3+2HCl=2NaCl+H2O+CO2↑ 【拓展延伸】①有气泡产生,生成蓝色沉淀 ②密封保存 【解析】 试题分析:【设计并实验】实验一:根据反应:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH,故取少量滤液于试管中,向试管这滴入适量的碳酸钠溶液,若无白色沉淀生成,则猜想二不成立 实验二:另取少量滤液于试管中,向其中加入过...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com