
【题目】质量守恒定律的发现,凝聚了许多科学家的心血。
材料一:早在17世纪,英国化学家波义耳在一个密闭容器中加热金属,得到了金属灰,然后打开容器盖,再次称量金属灰的质量,发现金属灰的质量比反应前的金属质量大。
村料二: 1756 年,俄国化学家洛蒙诺索夫在一个密闭的容器中加热金属锡,生成了白色的氧化锡,但容器和容器里的物质的总质量,在燃烧前后并没有发生变化。于是他认为在化学变化中物质的质量是守恒的,因此提出了质量守恒假说。
村料三: 1774 年,拉瓦锡用精确的定量实验在密封容器中研究氧化汞的分解与生成中各物质的质量之间的关系,再次对该假设加以论证。
请回答以下问题:
(1)拉瓦锡的实验证实了洛蒙诺索夫的假说,小明认为波义耳实验否定了该假说,你是否赞同小明的观点,请说明理由。_______
(2)小明建构了以下模型来从微观角度分析质量守恒定律,请你补充完整_______。
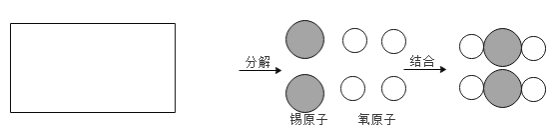
(3)为了进一步证实质量守恒定律,小明设计了如下四种实验方案,你觉得可行的是________(可多选)
A 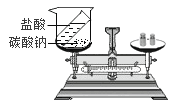 B
B 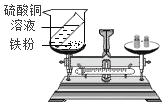
C 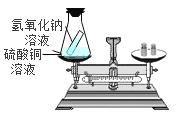 D
D 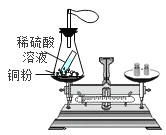
【答案】不赞同,金属灰的质量比反应前的金属质量大,是因为金属和氧气发生了反应,金属灰的质量等于反应前金属的质量加上参加反应的氧气的质量,符合质量守恒定律 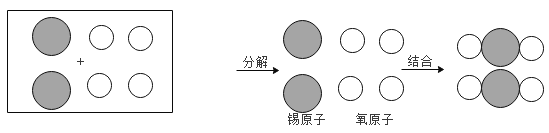 BC
BC
【解析】
(1) 不赞同小明的观点,理由:金属灰的质量比反应前的金属质量大,是因为金属和氧气发生了反应,金属灰的质量等于反应前金属的质量加上参加反应的氧气的质量,符合质量守恒定律;
(2)由于锡为金属,由原子直接构成,氧气由氧分子构成,每个氧分子由两个氧原子构成,所以图补充完整为:

(3) A、碳酸钠和盐酸反应生成二氧化碳气体,二氧化碳会逸出,不能验证质量守恒定律,不符合题意;
B、硫酸铜和铁反应生成硫酸亚铁和铜,能够验证质量守恒定律,符合题意;
C、氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,能够验证质量守恒定律,符合题意;D、稀硫酸和铜不能反应,不能验证质量守恒定律,不符合题意。
故选 BC。


科目:初中化学 来源: 题型:
【题目】如图所示表示治理汽车尾气所涉及反应的微观过程.下列说法正确的是( )
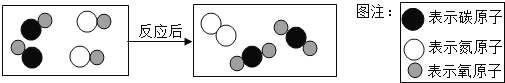
A.该反应使有毒气体转化为无毒气体
B.反应中原子、分子个数都不变
C.生成物的分子个数比为1∶1
D.图中有两种单质和两种氧化物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是实验室常用的装置。请据图回答:

(1)实验室若选用A、C装置制取和收集氧气,请写出有关反应的化学方程式_____。
(2)实验室选用B、E装置制取和收集二氧化碳,请在虚线框中画出用试管采用排空气法收集二氧化碳的装置图_____(只画试管和导气管);若将发生装置由B改为D,其优点是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是人类宝贵的自然资源,是生命之源。
(1)我国规定水质必须在感官性指标、化学指标、病理学指标等方面达标后方可以成为生活饮用水。各种指标的主要要求为:
A 不得呈现异色
B 不得有异味
C 水应澄清透明
D 不得含有细菌和病毒
①前两个指标可以通过活性炭的______作用而达到;
②自来水厂生产自来水的流程如图所示:
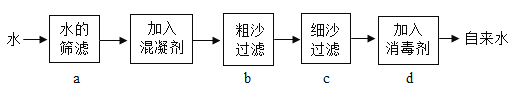
净化水时,C、D两个指标可通过上图的b、c和______过程而达到。
(2)天然水中含有许多杂质,实验室常用过滤方法除去水中不溶性杂质。过滤需要用到带铁圈的铁架台、烧杯、漏斗和______(填仪器名称),过滤后仍然浑浊的原因可能是______(写一条即可)。
(3)硬水给生活和生产带来很多弊端,我们常用______鉴别硬水和软水,生活中可以用_______的方法降低水的硬度。
(4)在电解水的实验中,两电极相连的玻璃管上方都会产生气体。一段时间后,与电源正、负极相连的两端产生的气体的体积比为______,请写出电解水的化学方程式_______。
(5)简阳市创建国家卫生城市,是一项提升居民生活品质与环境质量,改善城乡环境,保障居民身体健康的民生工程。下列观点正确的是(__________)
A 老城区重新安装排污管道,造成交通拥堵,弊大于利
B 生活污水逐步实现集中处理后排放
C 创建国家卫生城市是城区人的事,农村地广人少可以随意倾倒垃圾
D 农业上大量使用化肥和农药,不会造成水体污染
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了探究金属与酸的反应,某兴趣小组进行了以下实验:
(1)A小组研究影响金属与酸反应剧烈程度的因素,如图时20℃时相同质量的铁粉、铁片、铝片分别与足量稀盐酸完全反应,产生氢气的质量与时间的关系图。
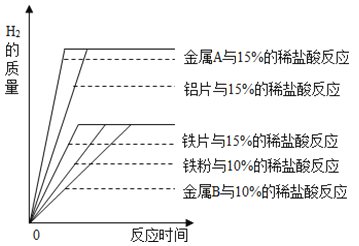
由此分析,归纳出影响金属与酸反应速率的因素有:金属的种类、_____和_____。
(2)金属铬(Cr)越来越受到人们的关注,B小组对Cr、Al、Cu的金属活动性顺序进行了探究,过程如下:
(提出假设)对三种金属的活动性顺序提出假设
a.Al>Cr>Cu b.Cr>Al>Cu c._____
(设计实验)同温下,取大小相同的金属薄片,分别投入到等体积、等浓度的足量稀盐酸中,观察现象,记录如下:
金属 | Cr | Al | Cu |
现象 | 反应缓慢,金属逐渐溶解 | 反应激烈,金属迅速溶解 | 无明显现象 |
(实验条件)实验前,打磨三种金属发生的是_____(填“物理”或“化学”)变化;上述实验使用等浓度的盐酸溶液的理由是_____。
(得出结论)原假设中正确的是_____(填假设中a、b或c),写出铬(铬与盐酸反应后显+2价)与盐酸反应的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下面三幅示意图分别表示不同的化学反应,但生成物中都有氯化钠。
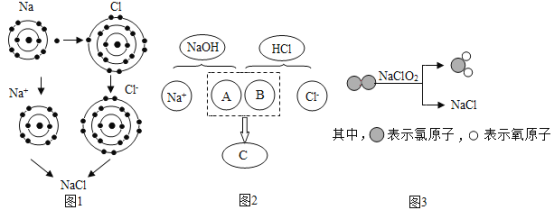
(1)图1是金属钠在氯气中燃烧生成氯化钠的微观示意图,氯化钠是由_____和_____ (填粒子符号) 构成的;写出图1生成氯化钠的化学方程式_____。
(2)图2的反应属于_____反应(填基本反应类型);图3反应的生成物是氯化钠和_____(填名称)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有碳酸钠和氯化钠的固体混合物12.6g,将该混合物加入到一定质量的稀盐酸中,恰好完全反应,生成二氧化碳质量4.4g,得到108.2g 氯化钠溶液。计算:
(1)原固体混合物中碳酸钠的质量是_____g。
(2)所用稀盐酸中溶质的质量分数及反应后所得溶液溶质质量分数_____(结果保留至0.1%)。
(3)蒸干108.2g氯化钠溶液得到固体质量大于12.6g,原因是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学用语表示:
(1)空气中含量最多的气体:_____。
(2)地壳中含量最高的金属元素:_____。
(3)2个氮气分子_____。
(4)硫酸亚铁是由_____和 _____ 构成的。
(5)氧化镁中镁元素的化合价为+2价:_____。
(6)氯气:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业铁红可用于生产颜料,其主要成分是 Fe2O3,还含有少量的FeO、Fe3O4。为了测定某种工业铁红样品中铁元素的质量分数,同学们进行了如下探究。
(查阅资料)
Ⅰ.草酸晶体(H2C2O43H2O)在浓硫酸的催化下受热分解,会生成二氧化碳、一氧化碳和水。
Ⅱ.碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳
Ⅲ.铁的常见氧化物中,铁元素的质量分数如下表所示:
铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
铁元素的质量分数 | 77.8% | 70.0% | 72.4% |
(设计与实验)小组同学设计了下图所示实验装置:
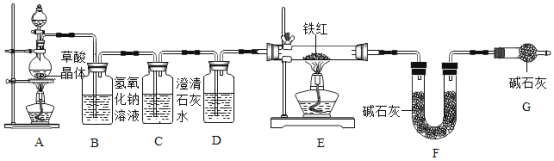
(1)为了保证进入E 中的气体是纯净、干燥的 CO,则 D 中的试剂名称为_____。
(2)C 装置的作用是_____。
(3)写出E 装置中发生反应的化学方程式(一个即可):_____。
(4)同学们称取 10.0g 铁红样品进行实验,根据资料信息推算,理论上铁红样品中铁元素质量的取值范围是_____。利用上述装置进行实验(装置气密性良好),并通过以下两种方法得出测定结果。
方法一:充分反应后,称量E 中得到的铁粉的质量,经计算求出铁元素的质量分数。
方法二:分别称量实验前后_____(填字母序号)装置的质量,经计算求出铁元素的质量分数。
(实验反思)
(1)如果缺少G 装置(不考虑其他因素),可能会导致利用方法二测定的样品中铁元素的质量分数偏小,原因是_____。
(2)从绿色化学的角度考虑,该实验装置的不足之处是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com