
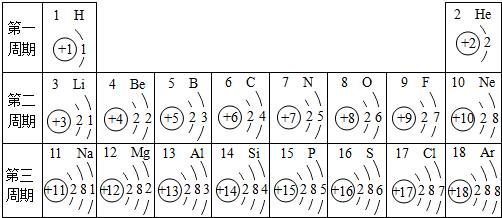
分析 (1)根据元素周期数与电子层数的关系、同一周期原子核外电子排布的变化进行分析解答;
(2)根据在第三周期中,元素类型的变化情况是:从左到右由金属元素过渡到非金属元素,并以稀有气体元素结束进行解答;镁原子的最外层电子数是2,铝原子的最外层电子数是3,在化学反应中镁原子更易失去电子;
(3)根据核外电子排布与与氖原子相同的阳离子可能是钠离子或镁离子以及铝离子,阴离子可能是氧离子、氟离子等进行解答;
(4)质子数为8的元素是氧元素,结合化学方程式的写法来分析.
解答 解:(1)在第三周期中,各原子结构的共同之处是原子核外电子层数相同;该周期中,从左到右,各原子核外电子排布的变化规律是最外层电子数依次增加;故填:原子核外电子层数相同;最外层电子数依次增加;
(2)在第三周期中,元素类型的变化情况是:从左到右由金属元素过渡到非金属元素,并以稀有气体元素结束;故填:金属;非金属;
从表可以看出,镁铝的电子层数相同,镁原子的最外层电子数是2,铝原子的最外层电子数是3,在化学反应中镁原子更易失去电子,因此在金属活动性顺序表中镁的活动性比铝的活动性强.故答案为:镁铝的电子层数相同,镁原子的最外层电子数是2,铝原子的最外层电子数是3,在化学反应中镁原子更易失去电子;
(3)核外电子排布与与氖原子相同的阳离子可能是钠离子或镁离子以及铝离子,阴离子可能是氧离子、氟离子;故填:Na+、Mg2+;
(4)由8号元素组成的单质是氧气,过氧化氢在二氧化锰的催化作用下分解为水和氧气,故填:氧气;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
点评 本题考查学生根据原子结构示意图分析总结元素周期律及对元素的性质与最外层电子数的关系的理解与掌握,并能在解题中灵活应用.


科目:初中化学 来源: 题型:选择题
| A. | 是9 mL | B. | 大于9 mL | C. | 小于9 mL | D. | 无法判断 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
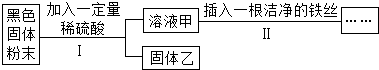
| A. | 若溶液甲呈浅绿色,则原黑色固体粉末中一定含有Fe | |
| B. | 若步骤Ⅱ中无明显现象,则固体乙中最多有五种物质 | |
| C. | 若步骤Ⅱ中有红色固体析出,则固体乙中一定无CuO | |
| D. | 若固体乙呈红色,则原固体中一定含有Fe和CuO |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分子很小 | B. | 分子之间有间隙 | C. | 分子在不断运动 | D. | 分子由原子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H202、H20都是氧化物,氧元素的化合价都是-2价 | |
| B. | NO2、N204中氮元素的化合价都是+4价,是同一化合物 | |
| C. | NH4NO3中氮元索有两种不同的化合价,分别是-3,+5 | |
| D. | 在原子团S042-中,各元素化合价代数和为零 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用锌粒和稀硫酸反应制取氢气 | |
| B. | 用燃着的木条鉴別氮气与二氧化碳 | |
| C. | 用稀盐酸除去铜粉中的铁粉 | |
| D. | 用无色酚酞试液鉴别稀氨水和蒸馏水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
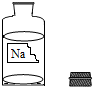 化学兴趣小组的同学在实验室发现一瓶保管不当,盛有无色溶液的试剂瓶,且标签破损(如图),其残缺的标签中只剩下“Na”字样.老师告诉他们,这瓶溶液中的溶质可能是氢氧化钠、氯化钠或碳酸钠.同学们很感兴趣,决定对其成分进行探究.
化学兴趣小组的同学在实验室发现一瓶保管不当,盛有无色溶液的试剂瓶,且标签破损(如图),其残缺的标签中只剩下“Na”字样.老师告诉他们,这瓶溶液中的溶质可能是氢氧化钠、氯化钠或碳酸钠.同学们很感兴趣,决定对其成分进行探究.| 实验 | 实验操作 | 主要实验现象 | 实验结论和解释 |
| Ⅰ | 取样于试管中,向其中滴加几滴无色酚酞溶液. | 无色溶液变红色 | 该溶液不可能是NaCl溶液.理由是NaCl溶液呈中性,不能使酚酞变色. |
| Ⅱ | 另取样于另一支试管中,向其中滴加足量的稀盐酸. | 产生大量的气泡 | 该溶液中为碳酸钠.有关反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com