
| A. | 乳酸是由碳元素、氢元素、氧元素构成的 | |
| B. | 乳酸的相对分子质量为90 | |
| C. | 乳酸中碳元素与氢元素的质量比为6:1 | |
| D. | 乳酸中碳元素的质量分数为40% |
分析 A、根据乳酸的组成进行分析判断即可.
B、根据相对分子的质量为组成分子的各原子的相对原子质量之和,进行分析判断.
C、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
D、根据化合物中元素的质量分数的计算方法来分析.
解答 解:A、乳酸是由碳元素、氢元素、氧元素组成的,故选项说法错误.
B、乳酸的相对分子质量为:12×3+1×6+16×3=90,故选项说法正确.
C、乳酸中碳、氢元素的质量比为(12×3):(1×6)=6:1,故选项说法正确.
D、乳酸中碳元素的质量分数为$\frac{12×3}{90}×100%$,故选项说法正确.
故选:A.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | 含有氧元素的化合物叫做氧化物 | |
| B. | 氯化钠的构成粒子是Na+和Cl- | |
| C. | 原子核是由质子和电子构成的 | |
| D. | NH3由一个氮元素和三个氢元素组成 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:计算题
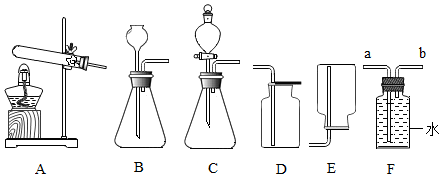
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
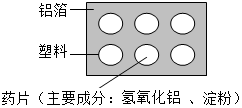 化学就在我们身边,它与我们的生活息息相关.
化学就在我们身边,它与我们的生活息息相关.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com