
| 实验步骤 | 实验现象 | 结论 |
| 实验步骤 | 实验现象 | 结论 |
| 取少量该液体于试管内并滴入几滴肥皂水震荡 | 出现泡沫 | 泡沫多的为软水,泡沫少的为硬水 |


科目:初中化学 来源: 题型:
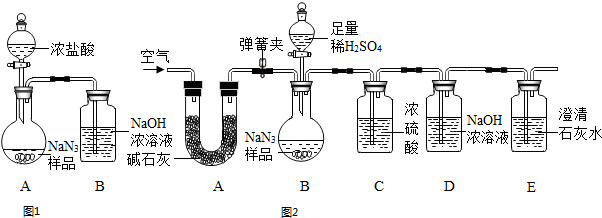
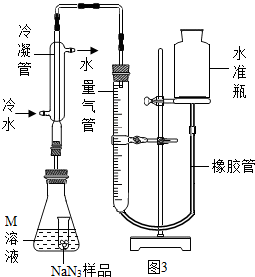
查看答案和解析>>
科目:初中化学 来源: 题型:
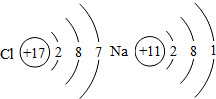 如图是两种元素的原子结构示意图.据此回答:
如图是两种元素的原子结构示意图.据此回答:查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验编号 | KClO3/g | 氧化物 | 产生气体的体积(mL) | 耗时(s) |
| 1 | 0.6 | -- | 67 | 1 800 |
| 2 | 0.6 | 0.2g 二氧化锰 | 67 | 36.5 |
| 3 | 0.6 | 67 | 89.5 |
| 实验装置 | 实验现象 | 实验分析 |
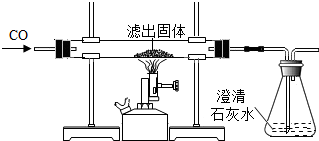 | 玻璃管中红色固体全部变黑 | 生成了铁 |
| 锥形瓶中石灰水变浑浊 | 产生了二氧化碳 |
| 铁粉 | 氧化亚铁 | 氧化铁 | 四氧化三铁 | |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 磁性 | 有 | 无 | 无 | 有 |
| 与CO | 不反应 | 反应 | 反应 | 反应 |
| 与稀盐酸 | 反应生成氯化亚铁和水 | 生成氯化铁和水 | 生成氯化亚铁、氯化铁和水 | |
| 与硫酸铜溶液 | 反应 | 不反应 | 不反应 | 不反应 |
| 步骤 | 实验操作 | 实验现象 | 结论和解释 |
| 1 | 用磁铁吸引剩余固体 | 剩余固体中没有氧化亚铁. | |
| 2 | 剩余固体中只有铁粉. |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
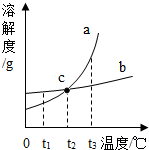 化学语言包括文字语言、符号语言、图表语言等.
化学语言包括文字语言、符号语言、图表语言等.| -2 |
| O |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
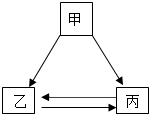 甲乙丙三种物质间通过一步反应能实现右图转化,下列选项中符合转化关系的是( )
甲乙丙三种物质间通过一步反应能实现右图转化,下列选项中符合转化关系的是( )| 选项 | 甲 | 乙 | 丙 |
| A | NaOH | NaCl | NaNO3 |
| B | CuO | CuCl2 | Cu(OH)2 |
| C | Na2CO3 | CO2 | CaCO3 |
| D | H2O2 | H2O | O2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com