
用微粒的观点解释下列事实,错误的是( )
A. 水的天然循环﹣分子在不断的运动
B. 食物变质一分子本身发生了变化
C. 汞做温度计的填充物﹣汞原子的体积受热变大,遇冷变小
D. 氧气支持燃烧,氮气不支持燃烧﹣不同种分子化学性质不同
科目:初中化学 来源:湖南省邵阳市邵阳县2019届九年级下学期中考二模化学试卷 题型:单选题
2018年3月,国务院总理李克强在政府工作报告中强调:“坚决打好蓝天保卫战”。 各地积极行动,落实措施。下列做法错误的是( )
A. 积极推广使用新能源公交车
B. 火力发电厂进行脱硫、控尘处理
C. 禁止化石燃料的使用
D. 限制、禁止燃放烟花爆竹
查看答案和解析>>
科目:初中化学 来源:四川省攀枝花市2019届九年级下学期中考模拟化学试卷 题型:科普阅读题
据新华网报道,南京某大学生因运动量大,一天喝了大瓶装的碳酸饮料6﹣7瓶,随后出现恶心、呕吐并昏迷症状等症状,后经抢救幸免于难.汽水是一种常见的碳酸饮料,家庭制备方法是:取一个干净汽水瓶,加入一定量冷开水(或冰水),再加入白糖及香精,然后加入2g碳酸氢钠(NaHCO3),搅拌溶解后,迅速加入适量柠檬酸(可用HA表示)并立即将瓶盖压紧即可.
(1)NaHCO3和柠檬酸反应产生CO2涉及的原理和碳酸钙与盐酸反应相似.碳酸钙与盐酸反应的化学方程式为_____.
(2)汽水中碳酸来源的化学方程式为_____.
(3)饮用汽水时,打开汽水瓶盖,立即冒出大量的气泡.为检验冒出的气泡中含大量CO2,可以采用的操作是_____,实验过程中将观察到的现象是_____.
查看答案和解析>>
科目:初中化学 来源:山东省烟台市龙口市2018-2019学年八年级上学期期末考试化学试卷 题型:实验题
如图分别是实验室净化天然水示意图和生活中的简易净水装置图。
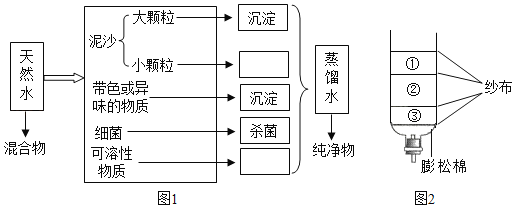
(1)在图1流程方框内从上到下依次填写的“关键词”是_____(填序号)。
a蒸馏 b蒸发 c结晶 d吸附 e过滤
(2)在图2所示的简易净水装置中,用小卵石、活性炭、石英砂做净水材料。要获得较好的净水效果,①②③处分别放置的是_____。
(3)图1得到的蒸馏水是_____(填“硬水”或“软水”)。我国规定1L合格的生活饮用水中,CaCO3的含量不超过450mg/L,则钙元素的含量不超过_____mg/L。
(4)分离混合物,首先要分析混合物的组成成分,寻找各成分的差异,然后利用其差异选择合适方法进行分离。如:过滤是分离_____不同的混合物的方法;蒸馏是分离_____不同的混合物的方法。
(5)水蒸馏的过程中,没有发生变化的是_____(填序号)。
①水分子的化学性质 ②水分子间的间隔 ③水分子的能量 ④水分子的构成
查看答案和解析>>
科目:初中化学 来源:山东省烟台市龙口市2018-2019学年八年级上学期期末考试化学试卷 题型:单选题
三种化合物CH4、C2H5OH、C2H2中若含有碳元素的质量相等,则CH4、C2H5OH、C2H2三种化合物中含有的氢元素的质量比为( )
A. 2:3:1 B. 4:3:1 C. 4:3:2 D. 1:1:1
查看答案和解析>>
科目:初中化学 来源:山东省烟台市龙口市2018-2019学年八年级上学期期末考试化学试卷 题型:单选题
有一种物质通过物理方法(物理变化)能得到两种不同的物质,该物质一定是( )
A. 单质 B. 化合物 C. 纯净物 D. 混合物
查看答案和解析>>
科目:初中化学 来源:四川省绵阳市2019届九年级下学期中考适应性(二)化学试卷 题型:填空题
化学与生活息息相关,知识源于生活。
①碘酒是家庭常备药,碘酒中的溶剂是_____(写化学式),炉具清洁剂中含有的碱是_____(写化学式)。
②我校食堂午餐食谱是:米饭、猪油炒白菜、红烧牛肉、炒鸡蛋,其中能提供富含蛋白质的食物有_____。
查看答案和解析>>
科目:初中化学 来源:江苏省苏州市2018届九年级上学期期中考试化学试卷 题型:单选题
试管在化学实验中常与其他仪器和药品同时使用(图中其他仪器和药品略去)。下列试管的朝向与实验项目相对应且正确的是




A B C D
A. 加热高锰酸钾制氧气
B. 向试管中加入粉末状药品的初始阶段
C. 排空气法收集氧气
D. 给液体加热
查看答案和解析>>
科目:初中化学 来源:江苏省常州市部分学校2019届九年级下学期中考模拟化学试卷 题型:综合题
过氧化镁(MgO2)是一种重要的化工原料,可用来处理被地下水污染的土壤,还可以用于配制牙膏,对牙齿有漂白和防过敏的作用。
(一)过氧化镁的性质
(1)过氧化镁是一种白色粉末。化学性质不够稳定,加热时会分解生成氧气和氧化镁;也不溶于水,但在水中会逐渐分解放出氧气。
(2)过氧化镁易溶于稀盐酸,发生反应:MgO2+2HCl==MgCl2+H2O2,同时放出大量的热。
(二)过氧化镁的制备
(1)煅烧:煅烧Mg2(OH)2CO3得到三种氧化物,其中一种常温下是气体,且能使澄清石灰水变浑浊,煅烧时反应的化学方程式为_____。检测煅烧过程碱式碳酸镁完全分解的方法是_____(写出具体的操作和现象)。
(2)转化:向所得固体中加双氧水充分搅拌,发生反应MgO+H2O2=MgO2+H2O
(3)分离:得到产品。
(4)测定:在生产过程中,过氧化镁中常常含有少量的氧化镁杂质(其他杂质不考虑)。
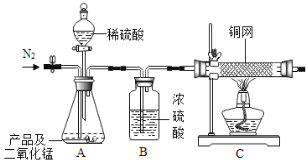
以下是某小组进行过氧化镁样品纯度检测的实验装置和实验步骤。
已知:a.MnO2与稀盐酸不反应
b.MgO+C Mg+CO↑
Mg+CO↑
实验前称取产品及二氧化锰共12g,先缓慢通入N2一段时间,加热铜网至红热后,再缓慢滴入过量稀盐酸,直至A中样品完全反应,继续缓慢通N2一段时间后停止加热。对锥形瓶中的剩余物过滤,洗涤,干燥,得到滤渣2g。
①样品完全反应后继续缓慢通N2的目的是_____;
②装置B的作用_____(填字母代号)
a.除去气体中水蒸气 b.便于观察和控制气流速度
③实验测得C装置中铜网增重1.6g,该产品中过氧化镁的含量为_____%(计算结果精确:到0.1%)
④经讨论,该小组又设计了下列3种方案,分别取5.0g产品进行实验,能确定MgO2质量分数的是_____(填序号)。
a.加热,使MgO2完全分解,测出剩余固体的质量
b.与足量炭粉在高温下充分反应,测出生成Mg的质量
c.先加足量稀盐酸,再加足量NaOH溶液,充分反应,测出Mg(OH)2质量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com