
| A. | 该物质一定含有碳、氢元素,可能含有氧元素 | |
| B. | 该物质一定不含氧元素 | |
| C. | 该物质中碳、氢元素的质量比为6:1 | |
| D. | 该物质分子中碳、氢原子个数比为1:1 |
分析 根据质量守恒定律,由生成物可以初步确定该物质中含有碳元素和氢元素,由生成的二氧化碳和水中碳、氢元素的质量和与该物质的质量进行对比,从而确定该物质的组成元素.化合物原子的个数比=$\frac{元素的质量比}{相对原子质量比}$,可以计算出该物质分子中碳原子和氢原子的个数比.
解答 解:4.4gCO2中含有碳元素的质量为:4.4g×$\frac{12}{12+16×2}$×100%=1.2g,1.8g水中含有氢元素的质量为:1.8g×$\frac{1×2}{1×2+16}$×100%=0.2g,生成物4.4g二氧化碳和1.8g水所含碳、氢元素的质量和=1.2g+0.2g=1.4g,1.4g<3g,该物质中含氧元素的质量为:3g-1.4g=1.6g,则该物质中一定含有碳、氢、氧三种元素.
A、由上述分析可知,该物质中一定含有碳、氢、氧三种元素,故选项说法错误.
B、由上述分析可知,该物质中一定含有碳、氢、氧三种元素,故选项说法错误.
C、由上述分析可知,该物质中碳、氢元素的质量比为1.2g:0.2g=6:1,故选项说法正确.
D、化合物原子的个数比=$\frac{元素的质量比}{相对原子质量比}$,则该物质分子中碳原子和氢原子的个数比为$\frac{1.2g}{12}$:$\frac{0.2g}{1}$=1:2,故选项说法错误.
故选:C.
点评 本题难度稍大,主要考查了质量守恒定律、化学式的计算,解题的关键是根据质量守恒定律确定确定物质的元素组成.


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
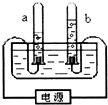 如图是实验室电解水的装置,请看图回答下列问题:
如图是实验室电解水的装置,请看图回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用手捏气球,可以使气球变瘪 | |
| B. | 墙内开花墙外香 | |
| C. | 100mL的水与100mL的酒精混合,所得溶液体积小于200mL | |
| D. | 将盐酸倒在大理石上可以观察到气泡 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 天平称物质质量为 12.52g | B. | 天平称物质质量为 12.0g | ||
| C. | 量筒量得液体体积为12.35mL | D. | 量筒量得液体体积为12.30mL |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com